
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
许多物质与身体健康有着密切关系,请结合所学知识,判断下列叙述中错误的是( )
|
| A. | 缺镁易患心血管病,缺碘易患甲状腺肿大 |
|
| B. | 在医疗上FeCl3常用作止血剂,ZnSO4常用作收敛剂 |
|
| C. | 葡萄糖、食盐、味精均可作食品添加剂 |
|
| D. | 苏丹红是一种呈红色的有机物,能当作辣椒红色素用于食品加工 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解100mL饱和食盐水,一段时间后,在阴极得到112mL H2(标准状况),此时电解质溶液(体积变化忽略不计)的pH为()
A. 13 B. 12 C. 8 D. 1
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物.
(1)为快速得到乙醇气体,可采取的方法是 ; 若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是 (填写编号);
a.取下小试管 b.移去酒精灯
c.将导管从乳胶管中取下 d.以上都可以
(2)盛Cu(OH)2悬浊液的试管中可能出现的现象为 .
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热.为了检验M的组成,进行下列实验.
①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
②经检验溶液中有Fe2+和Fe3+;
关于M 中铁元素价态的判断正确的是d(填写编号).
a.一定有+3价和+2价铁,一定无0价铁 b.一定有+3价、+2价和0价铁
c.一定有+3价和0价铁,一定无+2价铁 d.一定有+3和+2价铁,可能有0价铁
(4)若M的成份可表达为FeXOY,用CO还原法定量测定其化学组成.称取a g M样品进行定量测定,实验装置和步骤如下:

①组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧….正确的操作顺序是 (填写编号)
a.①⑤④③②⑥⑦⑧b.①③⑤④②⑦⑥⑧c.①⑤③④②⑥⑦⑧d.①③⑤②④⑥⑦⑧
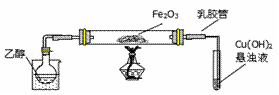
(5)若实验中每步反应都进行完全,反应后M样品质量减小b g,则FexOy中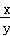 = .
= .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示物质结构的化学用语或模型图正确的是 ( )
A.H2O2的电子式:H+[
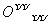
 ]2-H+ B.CS2的比例模型:
]2-H+ B.CS2的比例模型:
C.14C的原子结构示意图: D.CCl4的结构式:
D.CCl4的结构式:
查看答案和解析>>
科目:高中化学 来源: 题型:
把6mol铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为 ( )
A. 2mol B. 3mol C. 4mol D. 5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
有关 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )
A.除苯环外的其余碳原子有可能都在一条直线上
B.所有的原子都在同一平面上
C.12个碳原子不可能都在同一平面上
D.12个碳原子有可能都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生有机反应的化学方程式:
(2)试管C中苯的作用是 .反应开始后,观察D和E两试管,看到的现象为 .
(3)反应2~3min后,在B中的NaOH溶液里可观察到的现象是 .
(4)在上述整套装置中,具有防倒吸作用的仪器有(填字母): .

查看答案和解析>>
科目:高中化学 来源: 题型:
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
(1)冶炼铜的反应为:
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号).
(2)上述冶炼过程产生大量SO2.下列处理方案中合理的是 (填代号).
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I﹣氧化为I2:S2O82﹣+2I﹣=2SO42﹣+I2.
通过改变反应途径,Fe3 +、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
a.除去Al3+的离子方程式是 .
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 .证明炉渣中含有FeO的实验现象为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com