
 ��֪X��Y��Z��W�ֱ����ɶ�����Ԫ����ɵ�������������֮������ͼ��ʾ��ת����ϵ����X��һ�ֺ���18���ӵ�����Z��һ�ֺ���10���ӵ�������ش��������⣺
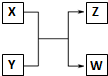
��֪X��Y��Z��W�ֱ����ɶ�����Ԫ����ɵ�������������֮������ͼ��ʾ��ת����ϵ����X��һ�ֺ���18���ӵ�����Z��һ�ֺ���10���ӵ�������ش��������⣺���� ��1��X��W�ֱ���������̬���ʷ��ӣ�ӦΪ�û���Ӧ��ӦΪ������ˮ�ķ�Ӧ����XΪF2��YΪH2O��ZΪHF��WΪO2��
��2����Y��W����ͬ����Ԫ���γɵĵ��ʷ��ӣ�һ��Ϊ����������ķ�Ӧ����ת���ϵ��֪��XΪH2S��YΪO2��ZΪH2O��WΪS��
��3����X��Y���Ǻ�2��ԭ�Ӻ˵���������Y�к���10�����ӣ�W�к���18�����ӣ���XΪHS-��YΪOH-��ZΪˮH2O��WΪS2-��
��4����W��һ�ֺ���22���ӵķ��ӣ�XΪ18����������������Ӧ������CO2��H2O��CO2����22�����ӣ��������⣬��WΪCO2��ZΪH2O��X��������Ԫ����ɵ��л����XΪ18���ӣ���XΪCH3CH3��
��� �⣺��1��X��W�ֱ���������̬���ʷ��ӣ�ӦΪ�û���Ӧ��ӦΪ������ˮ�ķ�Ӧ����XΪF2��YΪH2O��ZΪHF��WΪO2��X��Y��Ӧ�Ļ�ѧ����Ϊ2F2+2H2O=4HF+O2��
�ʴ�Ϊ��2F2+2H2O=4HF+O2��
��2����Y��W����ͬ����Ԫ���γɵĵ��ʷ��ӣ�һ��Ϊ����������ķ�Ӧ����ת���ϵ��֪��XΪH2S��YΪO2��ZΪH2O��WΪS��
�ʴ�Ϊ��H2O��
��3����X��Y���Ǻ�2��ԭ�Ӻ˵���������Y�к���10�����ӣ�W�к���18�����ӣ���XΪHS-��YΪOH-��ZΪˮH2O��WΪS2-��X��Y ֮�䷢����Ӧ�����ӷ���ʽΪHS-+OH-=S2-+H2O��
�ʴ�Ϊ��HS-+OH-=S2-+H2O��
��4����W��һ�ֺ���22���ӵķ��ӣ�XΪ18����������������Ӧ������CO2��H2O��CO2����22�����ӣ��������⣬��WΪCO2��ZΪH2O��X��������Ԫ����ɵ��л����XΪ18���ӣ���XΪCH3CH3��
�ʴ�Ϊ��CH3CH3��
���� ���⿼��Ԫ�ػ������ƶϡ�����10���ӡ�18�����������ʣ�Ԫ�������ɣ����û�ѧ����ȣ��ѶȺܴ��ƶ�Ԫ���������ǹؼ���ѧ��Ҫ��������10���ӡ�18����������֮��ķ�Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | I2����ˮ��������CCl4��HCl������ˮ | |
| B�� | ��ˮ�е��ܽ�ȣ�C2H5OH��CH3CH2CH2CH2OH | |
| C�� | ��ͬ����֮����ܽ� | |
| D�� | I2������KI��Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 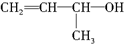 | B�� | CH2�TCH-CH3 | C�� |  | D�� | 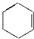 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
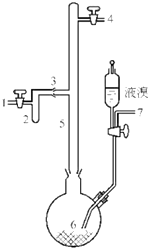 ���÷���������Ҫ�ɷ�ΪAl��������Fe��Si�ȣ��ȿ���ȡ�л��ϳɴ���AlBr3�ֿ���ȡ��ˮ������������[A12��SO4��3•18H2O]��
���÷���������Ҫ�ɷ�ΪAl��������Fe��Si�ȣ��ȿ���ȡ�л��ϳɴ���AlBr3�ֿ���ȡ��ˮ������������[A12��SO4��3•18H2O]���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ŨHNO3��ŨH2SO4�����Ծ���ǿ�������¶������������������� | |
| B�� | ¶���ڿ����У���������Һ������������ | |
| C�� | �����¶�����ͭ�Ͽ췴Ӧ | |
| D�� | ¶���ڿ����У���������Һ��Ũ�ȶ���С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��Ӧʱ��/min | n��MgSO4��/mol | n��CO��/mol | n��SO2��/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
| A�� | 0��2 min�ڵ�ƽ������Ϊ�� ��CO��=0.6 mol/��L•min�� | |
| B�� | 4 min��ƽ���ƶ���ԭ��������������м�����2.0 mol��SO2 | |
| C�� | �������¶ȣ���Ӧ��ƽ�ⳣ����Ϊ1.0��������ӦΪ���ȷ�Ӧ | |
| D�� | �����������䣬����ʼʱ������MgSO4��CO��Ϊ1.0 mol����ƽ��ʱn��SO2��=0.6 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
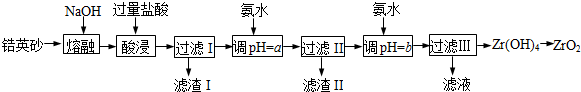
| �������� | Fe3+ | Al3+ | ZrO2+ |
| ��ʼ����ʱpH | 1.9 | 3.3 | 6.2 |
| ������ȫʱpH | 3.2 | 5.2 | 8.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӳɷ�Ӧ | B�� | ˮ�ⷴӦ | C�� | ������Ӧ | D�� | ��ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com