
【题目】2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地。1 mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,ΔE1=393.5 kJ,ΔE2=395.4 kJ,下列说法正确的是( )

A. 1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量
B. 石墨转化为金刚石属于物理变化
C. 金刚石的稳定性强于石墨的
D. 1 mol金刚石的能量大于1mol CO2的能量
【答案】A
【解析】由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJmol-1,②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJmol-1,利用盖斯定律将①-②可得:C(S,金刚石)=C(S,石墨)△H=-1.9kJmol-1,则A、根据以上分析可知C(s、石墨)=C(s、金刚石)△H=+1.9kJmol-1,A正确;B、石墨转化为金刚石是发生的化学反应,属于化学变化,B错误;C、金刚石能量大于石墨的总能量,物质的量能量越大越不稳定,则石墨比金刚石稳定,C错误;D、根据以上分析可知1mol金刚石和1mol氧气的总能量高于1molCO2的能量,D错误,答案选A。


科目:高中化学 来源: 题型:
【题目】为了验证SO2的性质,某同学利用输液管设计了如下微型实验:

请回答:
(1)仪器A的名称是_________________。
(2)装置C中NaOH的作用是_________________。
(3)下列说法正确的是_________________。
A.装置l、3、4中溶液均褪色,可证明SO2具有漂白性
B.装置2中石蕊试液只变红不褪色,证明SO2是一种酸性氧化物
C.反应结束后,可由a导管向装置中加水,将气体赶出后再拆装置
D.在a导管处用向下排空气法收集SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲和乙是双液原电池装置。由图可判断下列说法正确的是

A.甲图电池反应的离子方程式为Co(s)+Cd2+(aq)=Cd(s)+Co2+(aq)
B.由乙图可知,2Ag(s)+Co2+(aq)=Co(s)+2Ag+(aq)反应能够发生
C.盐挢的作用是形成闭合回路,并使两边溶液保持电中性,电池工作时盐桥中的阳离子移向正极
D.乙图中,当有lmol电子通过外电路时,正极有54克Ag析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用洗涤剂是污水中磷元素的重要来源(洗涤剂中常含有三聚磷酸钠),必须采取有效措施控制磷元素大量进入水体,其原因是
A. 使水体酸度大大增加,腐蚀桥梁、闸门等设备
B. 磷酸根进入水体,形成多种不溶性的磷酸盐,再吸附杂质,使河床抬高造成水患
C. 浮游生物得到养分,大量繁殖,死亡后腐败耗尽水中氧,使水质恶化
D. 磷酸盐有毒、致癌,不能进入水体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PM2.5中的某些物质,易引发光化学烟雾污染,光化学烟雾中含有NOx、OCS、CH2=CH-CHO、HCOOH、以及光气等二次污染物。水污染程度可通过测定水体中铅、铬等重金属的含量判断。
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______(用元素符号表示),CH2=CH-CHO分子醛基中碳原子杂化方式为____________。
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_________;光气(COCl2)各原子最外层都满足8电子稳定结构,则光气分子的空间构型为_________(用文字描述);
(3)1molHCOOH中含σ键和π键数目之比为______________。
(4)基态Cr原子核外电子排布式是_______,配合物[Cr(NH3)4(H2O)2] Cl3中心离子的配体为_______。
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=______(填数字)。若两个相邻面心的Kr原子的核间距为acm,用NA表示阿伏伽德罗常数,M表示Kr的相对原子质量。该晶体的密度计算式为______ g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地中海沿岸出产的一种贵重染料经化学分析,其主要组成的结构如图所示,下列说法不正确的是( )
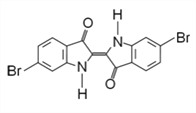
A. 属于烃的衍生物
B. 分子式为Cl6H8O2N2Br2
C. lmol该有机物与H2加成最多消耗9molH2
D. 该有机物溴元素检验可将有机物与碱液共热后,直接加入硝酸银溶液,观察是否有浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
某药厂在合成一种用于抑制血小板聚集的药物时使用到中间体有机物M,下图为有机物M(![]() )的合成路线:
)的合成路线:

已知:①B是石油裂解的主要产物,其产量用于衡量化工发展的水平。
②R—CHO+Rˊ—CH2COOR ![]()

回答下列问题:
(1)E的化学名称是___________;C的官能团名称为____________。
(2)反应条件①为_____________。
(3)C7H7C1→A的化学方程式为____________________。
A+D→E的反应类型为________________。
(4)F分子的结构简式为________,其最多有______个原子共平面。
(5)能同时满足下列条件的M的同分异构体共有______种。(不含立体异构)
①属于苯的对位二取代衍生物,且与M具有相同官能团;② 与苯环相连;③能够发生水解反应④能够发生银镜反应。
与苯环相连;③能够发生水解反应④能够发生银镜反应。
(6)参照上述合成路线,请填写方框中的空白,以完成制备聚丙烯酸甲酯的合成路线。______

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期。m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001 mol·L-1s溶液的pH为3, t是混合溶液,且该溶液具有漂白性。上述物质的转化关系如图所示。下列说法正确的是

A. 元素Y分别与W、X、Z形成的化合物中一定含有离子键
B. 离子半径:X<Y<Z
C. 由元素W、X组成的化合物中一定只含极性键
D. s为强酸,r为弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题共8分)现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图 。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:_____ _________。
(4)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com