
下列实验方案中,能测定Na2CO3和NaCl混合物中NaCl质量分数的是
A.取a克混合物与足量浓盐酸充分反应,通过排饱和NaHCO3溶液测得生成气体b升(已折算成标准状况)
B.取a克混合物与足量硝酸银溶液充分反应,过滤、洗涤、烘干,得b克固体
 C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤,称量得b克固体
科目:高中化学 来源:2016-2017学年四川省简阳市高二上学期期末化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.升高反应的温度,会使反应物的活化能迅速降低
B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C.用电解水的方法制取大量氢气可以缓解能源不足的问题
D.推广使用太阳能、风能等能源,有利于缓解温室效应
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上摸底考试四化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1 NaOH溶液:K+、Na+、SO42-、CO32-
B.能与铝反应放出氢气的溶液中:K+、SO42-、NO3-、NH4+
C.0.1 mol·L-1 FeCl3溶液:K+、NH4+、I-、SCN-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三上质检二化学卷(解析版) 题型:实验题
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3•CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中.从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为 (产物中只有一种酸根).请从反应原理分析不用盐酸浸出钴的主要原因 .
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: .
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三上质检二化学卷(解析版) 题型:选择题
下列关于有机化合物的说法正确的是
A.2-甲基丁烷也称异丁烷
B.三元轴烯( )与苯互为同分异构体
)与苯互为同分异构体
C.C4H9Cl有3种同分异构体
D.烷烃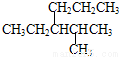 的正确命名是2-甲基-3-丙基戊烷
的正确命名是2-甲基-3-丙基戊烷
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期末化学试卷(解析版) 题型:计算题
将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3·bMn(OH)2·cH2O]。
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 ,反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 。
(2)为测定碱式碳酸锰组成,取7.390 g样品溶于硫酸,生成CO2 224.0 mL(标准状况),并配成500 mL溶液。准确量取10.00 mL该溶液,用0.0500 mol·L-1 EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2+ +H2Y2-=M nY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。
nY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期末化学试卷(解析版) 题型:选择题
一定条件下反应:R2O7n-+3S2-+14H+=2R3++3S+7H2O。则R2O7n-中R的化合价是
A.+2  B.+3 C.+4 D.+6
B.+3 C.+4 D.+6
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期末化学试卷(解析版) 题型:选择题
实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是
A.加水稀释 B.加少量NaOH溶液
C.降低温度 D.锌片改为锌粒
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团第二师华山中学高二上学期期末考试化学试卷(解析版) 题型:选择题
对于某一可逆反应,改变下列条件,一定能使化学平衡发生移动的是( )
A. 增加某反应物的质量 B. 使用催化剂
C. 降低反应体系的压强 D. 升高温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com