
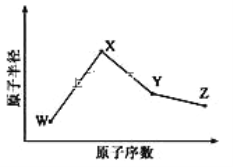
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差 1; 在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:
(1)X 元素位于元素周期表中位置为_____________。
(2)X 的单质和 Y 的单质相比,熔点较高的是____________(写化学式) 。 Z 所在族的简单氢化物中,沸点最高的是________(写化学式),原因为_________________________。
(3)W、X、Z 三种元素形成的化合物中化学键类型为________;X2W2的电子式为___________________。
(4)Y 与 Z 形 成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为__________________________。
(5)Z 的氧化物很多,其中一种黄绿色气体 M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性 。 M 的化学式为_____________。 M 可与 NaOH 溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为___________________。
(6)在 25°C、101kPa 下,已知 Y 的简单气态氢化物在氧气中完全燃烧后恢复至原状态, 平均每转移 1mol 电子放热 190kJ, 该反应的热化学方程式为__________________________________。
【答案】.第三周期, 第IA族SiHFHF 分子间能形成氢键离子键、共价键![]() SiCl4 +3H2O=H 2SiO3 +3HClClO26ClO2+6NaOH=NaCl+5NaClO3+3H2OSiH4 (g)+2O2 (g)=SiO2 (s)+2H2O(l) ΔH=—1520kJ/mol
SiCl4 +3H2O=H 2SiO3 +3HClClO26ClO2+6NaOH=NaCl+5NaClO3+3H2OSiH4 (g)+2O2 (g)=SiO2 (s)+2H2O(l) ΔH=—1520kJ/mol
【解析】
W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,则其质子数为18-10=8,故W为O元素;X和Ne原子的核外电子数相差1,原子半径大于O,故X为Na;由原子序数可以知道,Y、Z处于第三周期, Z的吸引电子的能力在同周期主族元素中最大,则Z为Cl,四种元素的最外层电子数之和为18,则Y的最外层电子数为18-6-1-7=4,所以Y为Si。
(1)X 元素为Na元素,位于元素周期表中位置为第三周期,第IA族;
(2)金属Na的熔点较低,Si属于原子晶体,熔点很高,故Si的熔点较高;Cl位于元素周期表第ⅦA族,F的电负性强,分子间可形成氢键,故HF沸点最高;
(3)W、X、Z 三种元素形成的化合物可能为NaClO,离子化合物,其中含有离子键和共价键;X2W2为Na2O2,离子化合物,电子式为:![]() ;
;
(4)Y与Z形成的化合物为SiCl4,和足量水反应,生成一种弱酸和一种强酸,应生成H2SiO3与HCl,该反应的化学方程式是:SiCl4 +3H2O=H 2SiO3 +3HCl;
(5)Z 的氧化物很多,其中一种黄绿色气体 M,其氧含量为 47.41%,则氯的含量为52.59%设M的化学式为ClxOy,则35.5x:16y=52.59:47.41,计算得x: y=1:2,则M为ClO2;M 可与 NaOH 溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,即NaCl 和NaClO3,则反应方程式为:6ClO2+6NaOH=NaCl+5NaClO3+3H2O;
(6)1mol SiH4完全燃烧转移的电子数为8mol,所以放热为190kJ×8=1520kJ,因此热化学方程式为SiH4 (g)+2O2 (g)=SiO2 (s)+2H2O(l) ΔH=—1520kJ/mol。


科目:高中化学 来源: 题型:
【题目】25℃时,用0.1mol·L-1HCl溶液滴定20.00mL 0.1mol·L-1BOH溶液所得的滴定曲线如图,下列说法正确的是
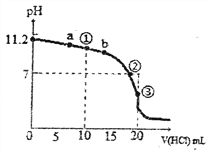
A. BOH为一元弱碱,滴定到点③时,该一元弱碱的电离平衡常数Kb约为10-5.6
B. 滴加盐酸的过程中,当溶液中c(BOH)=c(B+)时,可能出现在b点
C. 滴加盐酸的过程中水的电离程度逐渐增大,在②点时达到最大,后又逐渐减小
D. 点①所示溶液中:c(B+)+c(H+)>c(BOH)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下进行反应:COCl2(g)![]() Cl2(g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
Cl2(g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法正确的是( )
A. 保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol·L-1,则反应的ΔH<0
B. 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变
C. 保持其他条件不变,起始向容器中充入1.2 mol COCl2、0.60 mol Cl2和0.60 mol CO,反应达到平衡前的速率:v(正)>v(逆)
D. 保持其他条件不变,起始向容器中充入1.0 mol Cl2和0.8 mol CO,达到平衡时,Cl2的转化率小于60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.含有非金属元素的化合物一定是共价化合物
B.含共价键的化合物一定是共价化合物
C.含有金属元素的化合物可以是共价化合物
D.离子化合物一定含有金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曲酸和脱氧曲酸是非常有潜力的食品添加剂具有抗菌抗癌作用,其结构如图所示。下列有关叙述不正确的是

A. 曲酸的分子式为C6H6O4
B. 与脱氧曲酸互为同分异构体的芳香族化合物有4种(不考虑—O—O—键)
C. 曲酸和脱氧曲酸均能使酸性高锰酸钾溶液褪色
D. 脱氧曲酸能发生加成反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家对一碳化学进行了广泛深人的研究并取得了一些重要成果。
(1)已知:CO(g)+2H2(g) ![]() CH3OH(g) △H1=-90.1kJ/mol;
CH3OH(g) △H1=-90.1kJ/mol;
3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol
CO与H2合成CH3CH=CH2的热化学方程式为________。
(2)现向三个体积均为2L的恒容密闭容器I、II、Ⅲ中,均分别充入1molCO 和2mo1H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为Tl、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图1所示,其中只有一个容器中的反应已经达到平衡状态。

①5min时三个容器中的反应达到化学平衡状态的是容器_______(填序号)。
②0-5 min内容器I中用CH3OH表示的化学反应速率v(CH3OH)=_______。
③当三个容器中的反应均达到平衡状态时,CO的转化率最高的是容器___________。(填序号,下同);平衡常数最小的是容器_____________。
(3)CO常用于工业冶炼金属,在不同温度下用CO 还原四种金属氧化物,达到平衡后气体中![]() 与温度(T)的关系如图2所示。下列说法正确的是_____(填字母)。
与温度(T)的关系如图2所示。下列说法正确的是_____(填字母)。

a.工业上可以通过增高反应装置来延长矿石和CO接触面积,减少尾气中CO的含量
b.CO用于工业冶炼金属铬(Cr)时,还原效率不高
c.工业冶炼金属铜(Cu) 时,600℃下CO的利用率比1000℃下CO的利用率更大
d.CO还原PbO2的反应△H>0
(4)工业废水中含有甲醛,该厂降解甲醛的反应机理如图3所示,则X表示的粒子是_____,总反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用H2还原铁的氧化物并确定其组成的装置如图所示(Zn粒中往往含有硫化物等杂质,焦性没食子酸溶液可吸收少量氧气)。
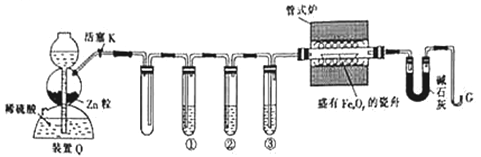
回答下列问题:
(1)装置Q(启普发生器)用于制备H2,还可用于_____(填字母,下同)。
A.生石灰与浓氨水制NH3 B.过氧化钠与水制O2
C.硫化铁固体与稀硝酸制H2S D.大理石与稀盐酸制CO2
(2)①②③中依次盛装的试剂为__________________。
A.KMnO4酸性溶液、浓H2SO4、焦性没食子酸溶液
B.焦性没食子酸溶液、浓H2SO4、KMnO4酸性溶液
C. KMnO4酸性溶液、焦性没食子酸溶液、浓H2SO4
KMnO4酸性溶液中发生反应的离子方程式为_____________。
(3)“加热管式炉”和“打开活塞K”这两步操作应该先进行的是__________,在这两步之间还应进行的操作是_______________。
(4)反应过程中G管逸出的气体是___________,其处理方法是___________。
(5)结束反应时,应该___________,待装置冷却后称量并记录相应数据。
(6)假设反应完全后瓷舟中的固体只有Fe单质,实验中测得了下列数据: ①瓷舟的质量为30.4g;②瓷舟和FexOy的总质量为42.0g;③反应前U形管及内盛物的总质量为98.4g;④反应后U形管及内盛物的总质量为102.0g。由以上数据计算并确定该铁的氧化物的化学式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com