
【题目】《Journal of Energy Chemistry》报导我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:

下列说法不正确的是
A.c为电源的负极
B.a极的电极反应式为:2C2O52- -4e- =4CO2 ↑+O2↑
C.①②中,捕获CO2时碳元素的化合价均未发生变化
D.转移l mol电子可捕获CO2 11.2 L(标况下)
【答案】D
【解析】
A. d电极上CO32-→C,得到电子,发生还原反应,所以d为阴极,则c为电源的负极,A正确;
B. a电极上C2O52-→O2,失去电子发生氧化反应,所以a为阳极,电极反应式为2C2O52- -4e- =4CO2 ↑+O2↑,B正确;
C. ①中CO2→C2O52-或②CO2→CO32-时C元素化合价均为+4价,所以C元素化合价均没有发生变化,C正确;
D. 根据图示a极生成O2,d极生成C,故该装置中总反应为CO2![]() C+O2,每捕获1molCO2转移4 mol电子,则每转移1mol电子捕获0.25molCO2,其在标准状况下体积为5.6L,D错误;
C+O2,每捕获1molCO2转移4 mol电子,则每转移1mol电子捕获0.25molCO2,其在标准状况下体积为5.6L,D错误;
故答案选D。


科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确,且存在对应关系的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将NaOH溶液逐滴滴加到AlC13溶液中至过量 | 先产生白色胶状沉淀,后沉淀溶解 | Al(OH)3是两性氢氧化物 |
B | NaHCO3溶液与NaAlO溶液混合 | 生成白色沉淀 | 结合H+的能力:CO32->AlO2- |
C | 向盛有Na2SiO3,溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至过量 | 试管中红色逐渐褪去,出现白色凝胶 | 非金属性:Cl>Si |
D |
| 白色固体先变为淡黄色,后变为黄色 | 溶度积常数:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯可用于制备二茂铁[Fe(C5H5)2,结构简式为![]() ],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法正确的是( )
],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法正确的是( )
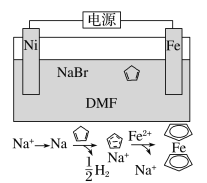
A.该电池工作是,镍连接的是电源的正极
B.可将该电池的DMF惰性有机溶剂更换为NaOH溶液
C.该反应的总反应方程式为Fe+2![]() +H2↑
+H2↑
D.溶液中的Na+离子不断的向Fe附近移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物的污染是目前科学家们研究的热点问题。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___。用尿素溶液也可吸收氮氧化物,研究表明,当混合气体中![]() =1时,总氮还原率最高,随着,
=1时,总氮还原率最高,随着,![]() 比值增大,总氮还原率降低的主要原因是___。
比值增大,总氮还原率降低的主要原因是___。
②在一个体积为1L的恒容密闭容器中充入1molCO2和1molNH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)![]() NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
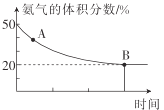
则A点时v正(CO2)___(填“>”“<”或“=”)B点时v正(CO2),原因是___。B点时,NH3的转化率为___。
③下列有关反应2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的说法正确的是___。
CO(NH2)2(s)+H2O(g)的说法正确的是___。
A.分离出少量的尿素,NH3的转化率将增大
B.反应达到平衡时,降低反应体系的温度,CO2的浓度减小
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高尿素的产率
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O2(g)=2NO2(g) △H1=akJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=bkJ·mol-1
6NO2(g)+O3(g)=3N2O5(g) △H3=ckJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)△H=___(用含a、b、c的代数式表示)kJ·mol-1。
(3)氮氧化物也可用碱液吸收。若NO和NO2的混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为___;已知常温下Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)![]() NaNO2(aq)+H2O(l)的平衡常数K=___。
NaNO2(aq)+H2O(l)的平衡常数K=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是

A.用图1装置可用于气体的发生、干燥和收集,如铜屑与稀硝酸反应制备NO
B.用图2装置制备Fe(OH)2并能较长时间观察其颜色
C.用图3装置可以验证FeCl3对H2O2分解反应有催化作用
D.用图4装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是原子序数为1~19的元素第一电离能的变化曲线(其中部分元素第一电离能已经标出数据)。结合元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列有关问题。
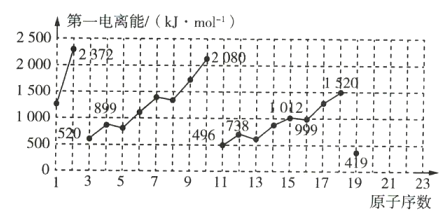
(1)碱金属元素中Li、Na、K的第一电离能分别为 _____________ ![]() 、 _____________
、 _____________ ![]() 、 _____________
、 _____________ ![]() 。
。
(2)同主族中不同元素的第一电离能变化的规律为: _____________ ,碱金属元素这一变化的规律与碱金属的活泼性的关系是 _____________ 。
(3)钙元素的第一电离能的数值范围为 _____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
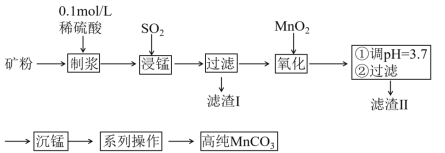
(1)对矿石进行粉粹的目的是_______;
(2)滤渣Ⅰ、Ⅱ分别为________、________;
(3)采用1%稀硫酸而不采用水混合矿粉制浆的原因是_________;不采用较浓H2SO4的原因是______;不直接采用H2SO4浸锰的原因是___________。
(4)浸锰的离子方程式为____________;
(5)“系列操作”为过滤、_________、干燥。
(6)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓溶液吸收,得到白色沉淀19.7g,则所得产品的纯度为________%(保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:xA(g)+yB(g)![]() zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度0.30mol/L。下列有关判断正确的是( )
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度0.30mol/L。下列有关判断正确的是( )
A.x+y<z
B.平衡向正反应方向移动
C.A的转化率降低
D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“异丙苯氧化法”生产丙酮和苯酚的合成路线如下,各反应的原子利用率均为100%。下列说法正确的是
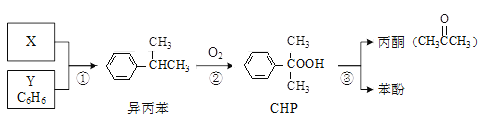
A. X的分子式为C3H8B. Y与异丙苯可用酸性KMnO4溶液鉴别
C. CHP与CH3COOH含有相同的官能团D. 可以用分液的方法分离苯酚和丙酮
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com