

| ||
| ||
| ||
| 太阳光 |
| ||
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
| △C |
| △t |
| 0.2mol |
| 1mol |
| 0.2mol |
| 2mol |
| 0.75mol/L-0.50mol/L |
| 6min |
| 0.25 |
| 6 |
| 0.05 |
| 0.05×0.12 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| c3(C) |
| c2(A).c(B) |
| c3(C) |
| c2(A).c(B) |
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,将16 mol N2与24 mol H2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是 ( )
2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是 ( )
A.达到平衡时,N2和H2的转化率之比为1:1
B.10分钟内v(H2)=0.35mol/(L·min)
C.平衡混合气体的密度为128g/L
D.平衡混合气体中,n(N2):n(H2):n(NH3)=1:3:2
查看答案和解析>>
科目:高中化学 来源:2010-2011学年黑龙江省高三上学期期末考试化学试卷 题型:选择题
将一定量A、B装入容积为1 L的恒温密闭容器中,发生反应:2A (s)+bB (g)  cC (g),1
min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为2.5x mol·L-1。下列说法正确的是
cC (g),1
min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为2.5x mol·L-1。下列说法正确的是
A.化学计量数的关系:b<c
B.容器的容积减小后,该反应的逆反应速率减小
C.若保持温度和容器的容积不变,充入氦气(不参与反应),平衡不发生移动
D.原容器中用B的浓度变化表示该反应在1 min内的速率为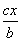 mol·L-1·min-1
mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2013届河北省高一下学期期末考试化学试卷 题型:填空题
(21分)工业上一般在恒容密闭容器中用H2和CO生产燃料甲醇,反应方程式为
CO(g)+2H2(g) CH3OH(g)△H
CH3OH(g)△H
(1)下表所列数据是反应在不同温度下的化学平衡常数(K)。
|
温度 |
250°C |
300°C |
350°C |
|
K |
2.041 |
0.270 |
0.012 |
①由表中数据判断△H 0(填“>”、“=”或“<“)
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 ,此时的温度为 。
(2)在100℃ 压强为0.1 MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇,达平衡时CO的转化率为50%,则100℃该反应的的平衡常数K= (用含a、V的代数式表示并化简至最简单的形式)。此时保持温度容积不变,再向容器中充入a mol CH3OH(g),平衡_____(向正反应方向、向逆反应方向)移动,再次达到新平衡时,CO的体积分数 。(减小、增大、不变)
(3)要提高CO的转化率,可以采取的措施是 。
A.升温 B.加入催化剂 C.增加CO的浓度
D.恒容充入H2 E.恒压充入惰性气体 F.分离出甲醇
(4)判断反应达到平衡状态的依据是(填字母序号,下同) 。
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(5)300°C,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
|
容器 |
甲 |
乙 |
丙 |
|
|
反应物投入量 |
1molCO、2moL H2 |
1molCH3OH |
2molCH3OH |
|
|
平 衡 时 的 数 据 |
CH3OH浓度(mol/L) |
c1 |
c2 |
c3 |
|
反应的能量变化 |
akJ |
bkJ |
ckJ |
|
|
体系压强(Pa) |
p1 |
p2 |
p3 |
|
|
反应物转化率 |
α1 |
α2 |
α3 |
请选择正确的序号填空(不定项选择)
(1)c1、c2、c3的关系表达正确的为______
A c3>2c1 B c1<c3<2c1 C c1=c2
(2)a、b、c的关系表达正确的为________
A c<2|△H| B a+b=|△H| C c=2b
(3)p1、p2、p3的关系不正确的为________
A p1=p2 B p2<p3<2p2 C p3>2p2
(4)a1、a2、a3的关系表达不正确的为________
A a1=a2 B a3< a2 C a1+a2=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com