
| A、18.4mol?L-1 34.7% |
| B、20.4mol?L-1 38.5%q2 |
| C、18.4mol?L-1 38.5% |
| D、20.4mol?L-1 34.7% |
| 700L |
| 22.4L/mol |
| 1531.25g |
| 900g/L |
| 531.25g |
| 1531.25g |
| 31.25mol |
| 1.7L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
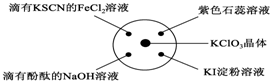 已知:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( )
已知:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( ) | 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
| C | 石蕊试液先变红后褪色 | Cl2具有漂白性 |
| D | KI淀粉溶液变蓝 | Cl2具有氧化性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y的离子具有相同的电子层结构 |
| B、X-比Y2-少一个电子层 |
| C、X+ 和Y2-具有相同的电子层结构 |
| D、X+比Y2-少一个电子层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铋能形成很稳定的气态氢化物 |
| B、铋的最高价氧化物对应的水化物的酸性比磷酸强 |
| C、铋单质可能具有良好的导电性并具有较大的密度 |
| D、铋的两种常见氧化物Bi2O3和Bi2O5,一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HClO═H++ClO- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、Al(OH)3?Al3++3OH- |
| D、NaH2PO4?Na++H2PO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeO |
| B、Fe3O4 |
| C、FeO?Fe3O4 |
| D、Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
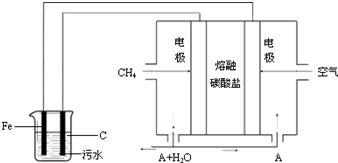 工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置示意图如图所示.
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置示意图如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com