
| ||
| 5min |
| 1.5mol |
| 3mol |


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
 2C(g)+2D(g);△H=Q.2min末达到平衡,生成0.8mol D.
2C(g)+2D(g);△H=Q.2min末达到平衡,生成0.8mol D.| c2(C)×c2(D) |
| c3(A)×c(B) |
| c2(C)×c2(D) |
| c3(A)×c(B) |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
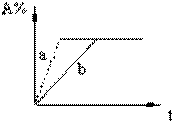 已知 3A(g)+2B(g)?C(s)+4D(g)△H<0.图中a、b表示在一定条件下,A的体积分数随时间t的变化.若使曲线b变为曲线a,可采取的措施是( )
已知 3A(g)+2B(g)?C(s)+4D(g)△H<0.图中a、b表示在一定条件下,A的体积分数随时间t的变化.若使曲线b变为曲线a,可采取的措施是( )查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知反应3A(g)+B(g)?2C(g)+2D(g)△H<0,如图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况.若想使曲线b(实线)变为曲线a(虚线),可采用的措施是( )
已知反应3A(g)+B(g)?2C(g)+2D(g)△H<0,如图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况.若想使曲线b(实线)变为曲线a(虚线),可采用的措施是( )| A、①②③ | B、④⑤ | C、③④⑤ | D、④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com