
| A、0.1molCuO |
| B、0.1molCuCO3 |
| C、0.1molCu(OH)2 |
| D、0.1molCu2(OH)2CO3 |


科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 |
| ①向装有硫化亚铁的试管中加入足量盐酸; | 溶液无浑浊,有大量臭鸡蛋气味的气体逸出 |
| ②将生成的硫化氢气体通入蒸馏水中达到饱和,取适量饱和溶液于试管中,不断振荡后,观察试管中的变化. | 试管中无明显的浑浊现象 |
| 实验步骤 | 实验现象 |
| 将新配制的硫化钠溶液分成两等份, 分别装入两支试管中 | |
| 向一支试管中直接加入盐酸; | 溶液稍显浑浊,有臭鸡蛋气味的气体逸出 |
| (1)向另一支试管中通入一定量氧气,观察溶液变化; (2)再加入盐酸; | (1)溶液没有明显变化; (2)溶液明显浑浊,有少量臭鸡蛋气味的气体逸出. |
| 实验步骤 | 预期现象和结论 |
| 向一装有硫化钠试管中加入足量的 溶液,以除去 沉淀,再将滤液装入试管中,加入盐酸. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
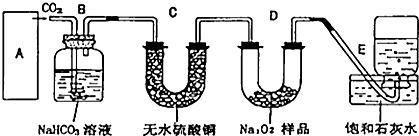

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液加KOH溶液生成红褐色沉淀,说明原溶液中有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯碱工业中通常使用阳离子交换膜将电解池的阳极区与阴极区隔开 | ||||
| B、合成氨工业中,将NH3不断液化分离有利于加快反应速率 | ||||
| C、在铜质餐具上镀银时,应将餐具与电源的正极相连 | ||||
D、高炉炼铁的主要反应为:Fe2O3+3CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
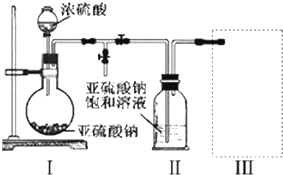
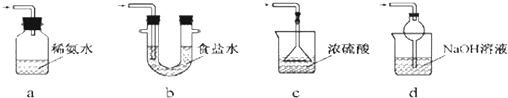
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com