
在同温同压下,下列各组热化学方程式Q2>Q1的是( )
| A.2H2(g) + O2(g)=2H2O(l);△H=-Q1 2H2(g) + O2(g)=2H2O(g);△H=-Q2 |
| B.S(g) + O2(g)=SO2(g);△H=-Q1 S(s) + O2(g)=SO2(g);△H=-Q2 |
C.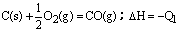 C(s) + O2(g)=CO2(g);△H=-Q2 C(s) + O2(g)=CO2(g);△H=-Q2 |
D.H2(g) + Cl2(g)=2HCl(g);△H=-Q1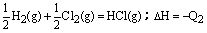 |
C
解析试题分析:反应放出或吸收的热量的多少,跟反应物和生成物的聚集状态有密切关系。A中两式仅生成物中水的状态不同,由于生成液态水比生成气态水放热多,所以Q1>Q2;B中两式仅硫的状态不同,由于固态硫变成气态硫要吸收热量,所以Q1>Q2;C中固态碳与氧气完全反应生成二氧化碳,放出的热量Q2应大于不完全燃烧时生成一氧化碳放出的热量Q1;D中二式各物质的量不同,有Q1=2Q2的关系,故本题的答案应为C。
考点:考查反应热的有关判断
点评:该是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力和方法的培养与训练,有利于培养学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确影响反应热大小的因素,然后结合题意灵活运用即可。


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:阅读理解
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
| 原料生产工艺过程 | ||||||||
| 乙炔 | CaCO3
| |||||||
| 乙烯 | 来源于石油裂解气 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.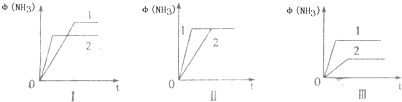
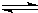 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.H2与O2总是按照质量比1∶8的关系发生化学反应
B.在同温同压下,H2的体积总是随着H2分子数的递增而增大
C.适宜的催化剂总是使化学反应的速率大幅度地提高
D.不同的元素,其金属性、非金属性各不相同。但全部元素的金属性、非金属性的差异是有规律的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实中可用元素周期律作解释的是…( )
A.H2与O2总是按照质量比1∶8的关系发生化学反应
B.在同温同压下,H2的体积总是随着H2分子数的递增而增大
C.MnO2可使KClO3加快分解
D.不同的元素,其金属性、非金属性各不相同。但在所有元素内,其金属性、非金属性的差异是有规律的
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省定州中学高考复习综合测试化学试卷(带解析) 题型:计算题
(10分)工业上目前使用两种方法制取乙醛:(1)乙炔水化法;(2)乙烯氧化法。下列两表提供生产过程中原料、反应条件、原料平衡转化率、产量等有关的信息情况:
表一:原料、反应条件、平衡转化率、日产量
| | 乙炔水化法 | 乙烯氧化法 |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
| | 原料生产工艺过程 |
| 乙炔 |  |
| 乙烯 | 来源于石油裂解气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com