
(8分)下面是测定硫酸铜结晶水的实验,按要求填空。
![]() (1)加热前应将晶体放在 研碎,加热时放在 中进行,加热失水后,应放在 中冷却。
(1)加热前应将晶体放在 研碎,加热时放在 中进行,加热失水后,应放在 中冷却。
(2)判断是否完全失去结晶水的方法是 。
(3)做此实验,最少应进行称量操作 次。
(4)下面是某学生的一次实验数据,完成计算,填入表中的空格。
坩埚质量 | 坩埚与晶
| 加热后坩埚
| 测量晶体中
| 误差(偏高
|
11.7g | 22.7g | 18.6g |
|
|
(5)这次实验中产生误差的原因可能是 (填序号)所造成的。
![]() A.硫酸铜晶体中含不挥发性杂质 B.加热过程中有晶体溅失
A.硫酸铜晶体中含不挥发性杂质 B.加热过程中有晶体溅失
![]() C.实验前晶体表面有湿存水 D.最后两次称量质量相差较大
C.实验前晶体表面有湿存水 D.最后两次称量质量相差较大
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:阅读理解
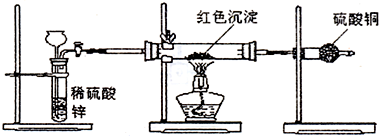
 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
| ||
| ||
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com