
| A. | 浓硫酸 | B. | 氢氧化钠 | C. | 硫酸亚铁 | D. | 浓盐酸 |
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,等质量的SO2和CO2密度比为11:16 | |
| B. | 同温同压下,等质量的SO2和CO2体积比为1:1 | |
| C. | 等物质的量的氢气和氦气在同温同压下具有相等的质子数 | |
| D. | 标准状况下气体摩尔体积就是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A. | 少量二氧化碳通入NaClO溶液中:2NaClO+CO2+H2O→Na2CO3+2HClO | |
| B. | 过量的 HCN滴入碳酸钠溶液中 HCN+Na2CO3→NaCN+NaHCO3 | |
| C. | 结合质子能力由强到弱的顺序为:HCO3->CN->C6H5O- | |
| D. | 常温下电离常数:Ka2(H2CO3)>Ka(C6H5OH)>Ka (HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
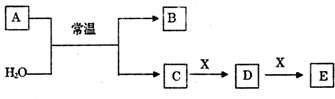
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子云通常是用小黑点来表示电子的多少 | |
| B. | 在同一能级上运动的电子,其运动状态肯定相同 | |
| C. | 能层序数越大,s电子云的半径越大 | |
| D. | 电子仅在激发态跃迁到基态时才会产生原子光谱 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2,O3,O4 | B. | 40Ca,40Ar | C. | Fe2+,Fe3+ | D. | 氕,氘,氚 | ||||
| E. | H2O,D2O,T2O | F. | H2,D2,T2 | G. | Na,Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4NO3=NH4++NO3- | B. | CH3COOH=H++CH3COO- | ||
| C. | NH3•H2O?NH4++OH- | D. | NaHCO3=Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液加入过量的氨水:Al3++4NH3•H2O═[Al(OH)4]-+4 NH4+ | |
| B. | 氯化亚铁溶液通入氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 硫酸铵溶液与氢氧化钡溶液混合:NH4++OH-═NH3↑+H2O | |
| D. | 铁与稀盐酸;2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com