
【题目】2,5-二羟基苯甲酸甲酯俗称龙胆酸甲酯,可由龙胆酸与甲醇酯化得到,是合成制药中的常见中间体。其结构如右图所示。
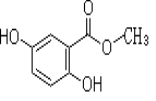
回答以下问题:
(1)龙胆酸甲酯所含官能团名称为 _________________
(2)龙胆酸甲酯的分子式为________________
(3)下列有关龙胆酸甲酯的描述,正确的是______________(填字母)。
a.能发生消去反应
b.能与氢气发生加成反应
c.能与浓溴水反应
(4)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式___________________ 。
(5)写出满足下列条件的龙胆酸的两种同分异构体的结构简式_________、____________。
① 能发生银镜反应; ② 能使FeCl3溶液显色;
③ 酯类 ④苯环上的一氯代物只有两种
(6)已知X及其它几种有机物存在如下转化关系,且测得C4H8含有一个支链,A的核磁共振氢谱图中有两个吸收峰。
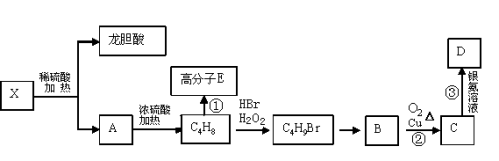
写出①的化学方程式____________________________________。
②的化学方程式______________________________________。
③化学方程式 ________________________________________。
写出X的结构简式________________。
【答案】
(1)酚羟基、酯基;
(2)C8H8O4;
(3)bc;
(4)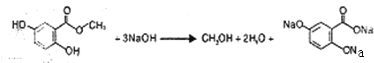 ;
;
(5)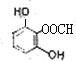 、
、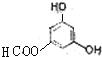 ;
;
(6)n(CH3)2C=CH2![]()
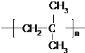 ;
;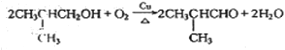 ;(CH3)2CHCHO+2Ag(NH3)2OH
;(CH3)2CHCHO+2Ag(NH3)2OH![]() (CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O;
(CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O;![]() 。
。
【解析】
试题分析:由X水解生成龙胆酸和A,据龙胆酸甲酯的结构简式可知,龙胆酸的分子式,A在浓硫酸作用下发生消去反应生成烯烃,C4H8含有一个支链,A为醇,A中有两种不同环境的氢原子,所以A为(CH3)3COH,X的结构简式是![]() ,B能经过两步氧化,则B为伯醇,即为(CH3)2CHCH2OH,据B生成C的反应条件可知,C为(CH3)2CHCHO,D为(CH3)2CHCOOH,
,B能经过两步氧化,则B为伯醇,即为(CH3)2CHCH2OH,据B生成C的反应条件可知,C为(CH3)2CHCHO,D为(CH3)2CHCOOH,
(1)由龙胆酸甲酯的结构简式可知,含酚羟基、酯基,故答案为:酚羟基、酯基;
(2)由龙胆酸甲酯的结构简式可知,分子式为C8H8O4,故答案为:C8H8O4;
(3)a.酚-OH、-COOC-均不能发生消去反应,故a错误;b.龙胆酸甲酯中有苯环,能与氢气发生加成反应,故b正确;c.龙胆酸甲酯中有酚的结构,能与浓溴水反应,故c正确;故答案为:bc;
(4)酚-OH、-COOC-均与NaOH反应,龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是 ,故答案为:
,故答案为: ;
;
(5)龙胆酸的一种同分异构体满足①能发生银镜反应,含-CHO;②能使FeCl3溶液显色,含酚-OH;③酯类,含-COOC-,④苯环上的一氯代物只有两种,说明苯环上有两种位置的氢,则符合条件的同分异构体的结构简式为 、
、 ,故答案为:
,故答案为: 、
、 ;
;
(6)根据上面的分析可知,反应①的化学方程式为n(CH3)2C=CH2![]()
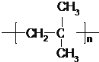 ,反应②的化学方程式
,反应②的化学方程式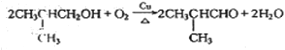 ,反应③的化学方程式为(CH3)2CHCHO+2Ag(NH3)2OH
,反应③的化学方程式为(CH3)2CHCHO+2Ag(NH3)2OH![]() (CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O,X的结构简式为
(CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O,X的结构简式为![]() ,故答案为:n(CH3)2C=CH2
,故答案为:n(CH3)2C=CH2![]()
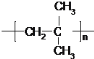 ;
;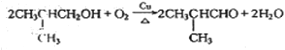 ;(CH3)2CHCHO+2Ag(NH3)2OH
;(CH3)2CHCHO+2Ag(NH3)2OH![]() (CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O;
(CH3)2CHCOONH4+2Ag↓+3NH3↑+H2O;![]() 。
。


科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:___________。
(2)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银.
①(H3PO2)中,磷元素的化合价为___________。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为:___________(填化学式);
③NaH2PO2是 正盐还是酸式盐?___________,其溶液显___________性(填“弱酸性”、“中性”、或者“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成PH3气体和Ba(H2PO2)2,后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式___________。
(4)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式___________;
②分析产品室可得到H3PO2的原因___________;
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是___________杂质。该杂质产生的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下:
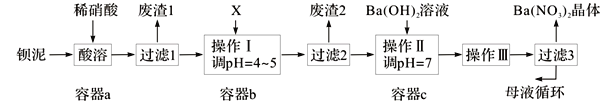
已知:i .Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7。
ii .Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小。
iii. Kap(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)Ba(FeO2)2中Fe的化合价是 。
(2)二氧化碳与水作用形成的碳酸在水中的电离常数Ka1=4.2×10-7 ,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 。
(3)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式和必要的文字说明提纯原理: 。
(4)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为: 。
(5)该厂结合本厂实际,选用的X为 (从下列选项中选择);废渣2为 (写出化学式)。
① BaCl2 ②Ba(NO3)2 ③BaCO3 ④ Ba(OH)2
(6)过滤3后的母液应循环到容器 中。(填“a”、“b”或“c”)
(7)称取w g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m g,则该Ba(NO3)2的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸,乳酸的结构简式为![]() 。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
(1)写出乳酸分子中官能团的名称 。
(2)一定条件下乳酸能发生的反应类型有______________ (填序号)。
A.水解反应
B.取代反应
C.加成反应
D.中和反应
E.氧化反应
F.酯化反应
(3)写出过量乳酸与碳酸钠溶液反应的化学方程式 。
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此有机生成物的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷催化裂解生成烷烃和烯烃,可按下列两种方式进行:C4H10→C2H4+C2H6;C4H10→C H4+C3H6某化学兴趣小组为了测定丁烷裂解气中CH4和C2H6的比例关系,设计实验如下图所示:
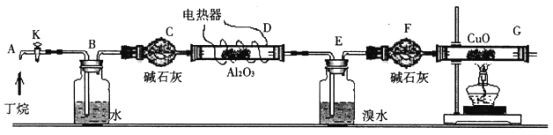
如图连接好装置后,需进行的操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……
注:CuO能将烃氧化成CO2和H2O;Al2O3是烷烃裂解的催化剂;G后面装置已省略。
(1)这三步操作的先后顺序是_________(填序号)
(2)简要叙述证明空气已排尽的操作方法______________________。
(3)假定丁烷完全裂解,且流经各装置中的气体能完全反应。当装置E和F的总质量比反应前增加了0.7g,G装置中固体质量比反应前减少了1.76g,则在丁烷的裂解产物中CH4和C2H6的物质的量之比n(CH4):n(C2H6)=______________。
(4)若对实验后E装置中的混合物再按以下流程进行实验:

![]()
①分离操作I、Ⅱ的名称分别是:I、_____________,Ⅱ、____________。
②Na2SO3溶液的作用是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1) Y在元素周期表中的位置为_____________________________.
(2) 上述元素的最高价氧化物对应的水化物酸性最强的是_____________________ (写化学式),非金属气态氢化物还原性最强的是_______________(写化学式)。
(3) Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________________ (写出其中两种物质的化学式))。
(4) ZX的电子式为_________________;ZX与水反应放出气体的化学方程式为__________________。
(5) 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),放电时,电池的正极反应 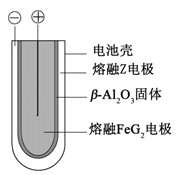
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下中的实验装置可用于制取乙炔。 请填空:
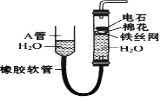
(1) 图中,A管的作用是_______________;制取乙炔的化学方程式是 。
(2)乙炔通入溴的CCl4溶液中观察到的现象是____________ ;乙炔发生了________反应。
(3)写出由乙炔制取聚氯乙烯的化学方程 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________________(已知:N2H4+H+![]() N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是___________。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为____________________________;
(2)A中的碳原子是否都处于同一平面?_________(填“是”或者 “否”);
(3)A是否存在顺反异构体?_________(填“是”或者“否”)。
(4)用系统命名法命名A为______________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com