
| A. | 纯碱、氯水、氢氧化钠、干冰 | B. | 醋酸、盐酸、铜、氨气 | ||
| C. | 石灰石、石油、水、硫酸钡 | D. | 烧碱、海水、氯化钠、氯气 |
分析 纯净物是指由同种物质组成的,混合物是指由不同种物质组成的,电解质是指在水溶液里或熔化状态下能够导电的化合物,非电解质是指在水溶液里和熔化状态下都不能够导电的化合物.据此可以分析各个选项中各种的所属类别.
解答 解:A.纯碱、氯水、氢氧化钠、干冰分别属于纯净物、混合物、电解质、非电解质,故A正确;
B.铜是单质,既不是电解质又不是非电解质,故B错误;
C.硫酸钡是电解质,熔融时可以导电,故C错误;
D.氯气是单质,既不是电解质又不是非电解质,故D错误.
故选A.
点评 本题考查纯净物、混合物、电解质和非电解质的概念,难度不大,需要对相关概念有深刻的理解,并能对相关属类的物质有清晰的理解,这要求在学习概念时,既要理解概念,又要能举出典型例子.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢硫酸显弱酸性:H2S?2H++S2- | |
| B. | Na2CO3水溶液显弱碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 用铜电极电解饱和NaCl溶液:阳极反应式是:2Cl--2e-=Cl2↑ | |
| D. | 用稀硝酸洗去试管中的银镜:3Ag+NO3-+4H+=3Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 碘的四氯化碳溶液可用萃取的方法分离出四氯化碳 | |
| D. | 配制稀硫酸时,先向烧杯中注入适量蒸馏水,再缓慢注入浓硫酸,并用玻璃棒不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在1 min时:c(SO3)+c(SO2)=1.0L/mol | |
| B. | 2 min 内:v(SO2)=0.25moL/(L•min) | |
| C. | 若再充入2mol SO3,达平衡时SO3%(质量分数)减小 | |
| D. | 反应条件相同,若起始时向反应容器中充入2mol SO3,平衡时反应吸热0.75a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
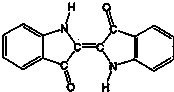
| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 该物质是天然高分子化合物 | D. | 靛蓝中含苯环,属于芳香化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤ | B. | ①②⑤ | C. | ④⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
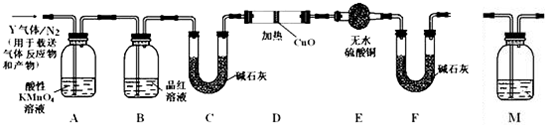
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | 由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| ② | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| ③ | Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- | |
| ④ | FeCl2溶液:K+、Na+、SO42-、AlO2- |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com