
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 蔬菜表面洒少许福尔马林,可保鲜和消毒 | |
| B. | 绿色食品就是不使用化肥农药,不含任何化学物质的食品 | |
| C. | 光催化水制氢比电解水制氢更节能环保 | |
| D. | 光化学烟雾不会引起呼吸道疾病 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 mL 1 mol•L-1的KNO3溶液 | B. | 50 mL 1 mol•L-1的Fe(NO3)3 | ||
| C. | 1 L 0.5 mol•L-1的Mg(NO3)2溶液 | D. | 1 L 0.5 mol•L-1的Ba(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素A的原子核外有2个电子 | |
| B. | 工业上常用电解C的盐溶液的方法制备元素C的单质 | |
| C. | 在所有非金属的氢化物中,元素E的气态氢化物最稳定 | |
| D. | 元素C的最高价氧化物对应的水化物的碱性比D的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2<P2O5<Cl2O7<SO3 | B. | SiO2<P2O5<SO3<Cl2O7 | ||
| C. | P2O5<SiO2<SO3<Cl2O7 | D. | P2O5<SO3<Cl2O7<SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.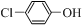 )的废水可以通过构成微生物电池除去,其原理如图所示.①B是电池的负极(填“正”或“负”);②A极的电极反应式为
)的废水可以通过构成微生物电池除去,其原理如图所示.①B是电池的负极(填“正”或“负”);②A极的电极反应式为 +2e-+H+═
+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com