
����Ŀ��Fe2+��Fe3+��O22����CN����F�����л����ӵ��γɵĻ�������й㷺��Ӧ�ã� 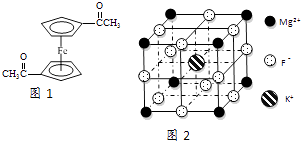
��1��C��N��Oԭ�ӵĵ�һ�������ɴ�С��˳����
��2��Fe2+��̬��������Ų�ʽΪ ��
��3����������ï���dz������Ϳ��������ṹ��ͼ1��ʾ����������̼ԭ�ӵ��ӻ���ʽ�� ��
��4�������K3Fe��CN��6�����ڵ��Ӵ������������������廥Ϊ�ȵ������һ�ַ��ӵĻ�ѧʽΪ �� ��֪��CN��2��ֱ���ͷ��ӣ������жԳ��ԣ���CN��2�Цм��ͦҼ��ĸ�����Ϊ ��
��5��F����������Fe3+�γ�[FeF6]3�� �� ��������Mg2+��K+�γ�һ��������ϵ�����Ӿ��壬�˾���Ӧ���ڼ������ṹ��ͼ2��ʾ���þ���Ļ�ѧʽΪ ��
���𰸡�
��1��N��O��C
��2��1s22s22p63s23p63d6
��3��sp2��sp3
��4��CO��N2|4��3
��5��KMgF3
���������⣺��1��ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ�����C��N��O����Ԫ�صĵ�һ���������ɴ�С��˳����N��O��C��
���Դ��ǣ�N��O��C����2������26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ���������Ų�ʽΪ��1s22s22p63s23p63d64s2��ʧȥ2�����ӱ��Fe2+�����̬��������Ų�ʽ��1s22s22p63s23p63d6��
���Դ��ǣ�1s22s22p63s23p63d6����3��������Cԭ����̼̼˫����̼̼������ʽ���ڣ���̼ԭ�ӵ��ӻ���ʽ��sp2��sp3��
���Դ��ǣ�sp2��sp3����4��CN���к�������ԭ���Ҽ۵�������10��������CN����Ϊ�ȵ������һ�ַ��ӵĻ�ѧʽ��CO��N2��
��CN��2��ֱ���ͷ��ӣ����жԳ��ԣ��ṹʽΪ��N��C��C��N��1��������1���Ҽ���1�������к���1���Ҽ���2���м������ԣ�CN��2�Цм��ͦҼ��ĸ�����Ϊ4��3��
���Դ��ǣ�CO��N2��4��3����5��������F��������Ŀ=12�� ![]() =3��Mg2+������Ŀ=8��
=3��Mg2+������Ŀ=8�� ![]() =1��K+������Ŀ=1���ʾ��廯ѧʽΪ��KMgF3��
=1��K+������Ŀ=1���ʾ��廯ѧʽΪ��KMgF3��
���Դ��ǣ�KMgF3��


 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���������У�����ȷ���ǣ�������
A.��ʪ���pH��ֽ��ϡ��Һ��pHֵ���ⶨֵƫС
B.������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС
C.�ζ�ǰ�ζ����������ݣ��յ����ʱ�����ݣ��������ƫС
D.�ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ��������������У������¶�ֵƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�Ͻ�㷺���ں��չ�ҵ�����и�����л��������Ʊ�ͭ������Ʒ�Ĺ������£�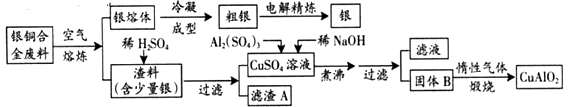
(ע��Al(OH)3��Cu(OH)2��ʼ�ֽ���¶ȷֱ�Ϊ450���80��)
��1����������B�����Ϊ�������ɹ���B�Ĺ����У������NaOH�ļ���������NaOH�����������������ķ�Ӧ�����ӷ���ʽΪ��
��2��������չ�����һ����Ӧ�Ļ�ѧ����ʽ����
��3������ͭ�Ͻ���ͭ����������Ϊ64%��������5��0kg�����е�ͭ����ȫת��ΪCuAlO2 �� ������Ҫ1��0mol��L-1��Al2(SO4)3��Һ L��
��4��ijͬѧ��FeCl3��Һ����H2S���õ��������˺�����ʯīΪ�缫����һ�������µ����Һ��
��FeCl3��H2S��Ӧ�����ӷ���ʽΪ��
�ڵ�����H+�������ŵ����H2 �� �����ĵ缫��ӦΪ��
���ۺϷ���ʵ��II��������Ӧ����֪��ʵ�������������ŵ㣺
H2S��ԭ��������100%����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��0.1mol/L��HA��Һ�� ![]() =1010 �� 0.01mol/L��BOH��ҺpH=12����ش��������⣺
=1010 �� 0.01mol/L��BOH��ҺpH=12����ش��������⣺
��1��HA�����ǿ����ʡ���������ʡ�����ͬ����BOH�� ��
��2��HA�ĵ��뷽��ʽ�� �� ������ˮ�������c��H+��=mol/L
��3���ڼ�ˮϡ��HA�Ĺ����У�����ˮ�������Ӷ���С����������ĸ����
A.![]()
B.![]()
C.c��H+����c��OH�����ij˻�
D.c��OH����
��4��������������ʵ���Ũ�ȵ�HA��Һ��BOH��Һ��Ϻ����Һ���ԣ��������ӷ���ʽ������ԭ�� �� �����Һ�и�����Ũ���ɴ�С��˳���� ��
��5��������pH=12��BOH��Һ100mL����0.01mol/L NaHSO4ʹ��Һ��pHΪ11���������Һ����仯���Բ��ƣ���Ӧ�� NaHSO4mL��������С�����һλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ���������������A��B��C��D��E��F����Ԫ�أ�����A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ�ӵ���ͬ��DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�E��Cλ��ͬһ���壬F��ԭ������Ϊ29��
��1��Fԭ�ӻ�̬����Χ��������Ų�ʽΪ ��
��2����A��B��C����Ԫ���У���һ��������С�����˳��������Ԫ�ط��Żش𣩣�
��3��Ԫ��B�ļ���̬�⻯��ķе������ڣ����ڣ�Ԫ��A�ļ���̬�⻯��ķе㣬����Ҫԭ���� ��
��4����A��B��C�γɵ�����CAB����AC2��Ϊ�ȵ����壬��CAB���ĽṹʽΪ ��
��5����Ԫ��A��E���γɵij����������У�Aԭ�ӹ�����ӻ�����Ϊ ��
��6����B��C��D����Ԫ���γɵĻ����ᄃ��ľ�����ͼ��ʾ����û�����Ļ�ѧʽΪ �� 
��7��FC�ڼ�������������ת��ΪF2C����ԭ�ӽṹ�ĽǶȽ���ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���縡ѡ���۷�����������ˮ�Ĺ���ԭ����ͼ������˵����ȷ���ǣ�������
A.Ϊ��ǿ��ˮ�ĵ���������������ˮ�м���������ҵ��ʳ��
B.ͨ���������ĵ缫��ӦʽΪ��CH4-8e-+10OH-=CO32-+7H2O
C.�����ʯī�缫����22.4L���壬������0.25mol����
D.���缫�ĵ缫��ӦʽΪ��Fe-3e-=Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)Ϊ�˼���ͳ�ȥ�±��еĸ�������(�������Ϊ����)����Ӣ���ѡ���ʵ��ļ����Լ����Ӣ���ѡ���ʵ��ij����Լ�������ѡ�Ĵ�����ĸ������Ӧ�Ŀո��ڡ�
���� | �����Լ� | �����Լ� |
(��)����(��ϩ) | ________�� | ________�� |
(��)�ƾ�(ˮ) | ________�� | ________�� |
�ټ����Լ���
A����ˮ����ͭ B�����Ը��������Һ
C��ˮ D������������Һ
�ڳ����Լ���
a����ˮ����ͭ b������
c�����Ƶ���ʯ�� d����ˮ
����ʱ����ϩ������Ӧ�Ļ�ѧ����ʽΪ____________________��
(2)��ͼ�������Թ����ȼ���2 mL 95%���Ҵ�������ҡ���»�������3 mLŨ���ᣬ�ټ���2 mL���ᣬ���ҡ�ȡ���ͼ���Ӻ�װ�ã��þƾ��ƶ����Թ�С�����3��5 min���ô����ȣ����۲쵽���Թ�������������ʱֹͣʵ�顣
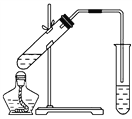
�Իش�
�����Թ���ͨ������________��Һ��ʵ�����ɵ��������������ܶȱ�ˮ________������������ζ��Һ�塣�������Թ����������������IJ���Ϊ(ֻ������)________����Ӧ�м���Ũ�����������_____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��CuFeS2������ͭ������Ҫ�����Ұ������ױ����Ϊ�ƽ��ֳ����˽�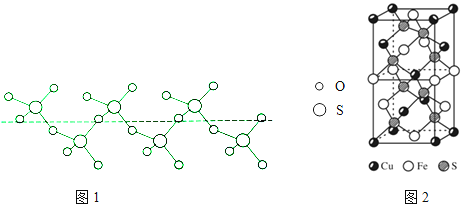
��1����ұ����ͭ��Ĺ����У�������Cu2O��Cu2S��Ӧ����Cu���ʣ���Ӧ�Ļ�ѧ����ʽ��
��2��Sλ�����ڱ��С� �壬����Ԫ���⻯���У�H2Te��H2S�е�ߵ�ԭ���� ��H2O��H2Te�е�ߵ�ԭ����
��3��S��+4��+6���ּ�̬��������ش��������⣺
�����й�����̬SO3��SO2��˵���У���ȷ���ǡ� ����
A������ԭ�ӵļ۲���Ӷ���Ŀ��� B�����Ǽ��Է���
C������ԭ�ӵŶԵ�����Ŀ��� D�������м��Լ�
�ڽ���Һ̬SO3��ȴ��289.8Kʱ���̵õ�һ������״�����ṹ�Ĺ��壬��ṹ��ͼ1���˹�̬SO3��Sԭ�ӵ��ӻ���������ǡ�
��4��Cu��+1��+2���ּ�̬�Ļ�����ش��������⣺
��Cu+�ļ۲�����Ų�Ϊ�� ����Cu2+�С� ����δ�ɶԵ��ӣ�
�����Ƶ�Cu��OH��2�ܹ��ܽ��ڹ���Ũ����Һ�У���Ӧ�����ӷ���ʽ�ǡ�
��5��CuFeS2�ľ�����ͼ2��ʾ����������a=0.524nm��c=1.032nm��CuFeS2�ľ�����ÿ��Cuԭ���롡 ����Sԭ����������ʽ���㾧���ܶ� ��=�� �� gcm��3 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��Ϊ��ѧ��ѧ�����Ĵ����A�ǵ��ʣ�����֮������ͼ�ķ�Ӧ��ϵ��
��1����A�ǵ���ɫ���壬C��D���������C������������Ҫ���ʣ�����C���ʿɵõ��м�ֵ�Ļ�ѧƷ��д������1�����1���ε����� ��
��2����B����̬�⻯�C��D���������һ���ɹ⻯ѧ������Ⱦ��B��C��һ�������·�Ӧ���ɵ�A�Ǵ�����Ҫ�ɷ֣�д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����D���ʾ������ԣ��ڢ۷�Ӧ��Ҫ��ǿ����Һ���ܷ�Ӧ��ͨ�������һ����������ЧӦ����Ҫ���壮�жϵ���A��Ԫ�������ڱ��е�λ���� ��д�ܷ�Ӧ���ӷ���ʽ ��
��4����A��̫���ܵ���õĹ�����ϣ�C��DΪ���Σ������������ơ������Ԫ��Ϊͬһ���壬����Һ���Լ��ԣ�д���ڷ�Ӧ�Ļ�ѧ����ʽ�� ��D�Ļ�ѧʽ�ǡ� ��
��5����A��Ӧ����㷺�Ľ������ܷ�Ӧ�õ�A���ڢݷ�Ӧ���õ�ͬһ�ַǽ������ʣ�C����Һ����ʴ��ӡˢͭ��·�壬д�÷�Ӧ�����ӷ���ʽ�� ��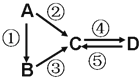
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com