
(15��)̼�͵��Ļ���������������������������ء�
��1����һ���¡������ܱ������з�����Ӧ�� Ni(s)+4CO(g) 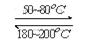 Ni(CO)4(g)��
Ni(CO)4(g)�� H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99��9���ĸߴ������Ը÷�Ӧ��˵����ȷ����
H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99��9���ĸߴ������Ը÷�Ӧ��˵����ȷ����
(����ĸ���)��
| A������Ni���������CO��ת���ʣ�Ni��ת���ʽ��� |
B����С�����ݻ���ƽ�����ƣ� H��С H��С |
| C����Ӧ�ﵽƽ�����CO�ٴδﵽƽ��ʱ��CO������������� |
| D����4vNi(CO)4=v(CO)ʱ�������л�������ܶȲ���ʱ������˵����Ӧ�Ѵﻯѧƽ��״̬ |
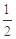 O2(g)==CO(g)
O2(g)==CO(g)  H= -Q1 kJ��mol-1
H= -Q1 kJ��mol-1 H= -Q2 kJ��mol-1
H= -Q2 kJ��mol-1 H= -Q3 KJ��mol-1
H= -Q3 KJ��mol-1 H= kJ��mol-1��
H= kJ��mol-1��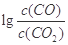 ���¶ȣ�t���Ĺ�ϵ����ͼ��
���¶ȣ�t���Ĺ�ϵ����ͼ��
��15�֣�
��1��C ��3�֣�
��2����(2Q2��2Q1��Q3) kJ��mol��1��2Q1��2Q2��Q3��kJ��mol��1 ��3�֣�
��3��Cr2O3 ��3�֣� 10��12 ��2�֣�
��4��NO2��NO3����e����N2O5 ��2�֣� 224��2�֣�
���������������1��A��Ni�ǹ��壬Ũ��Ϊ�������ı�������ƽ����Ӱ�죬��Ӧ���ת���ʲ��䣬����B��һ���¶��¸����Ļ�ѧ����ʽ�ġ�H��������ƽ���ƶ����ı䣬ֻ�뷽��ʽ����д��ʽ�йأ�����C�����������Ϊ���º��ݡ�Ni�ǹ���������ӦΪ���������С�ķ�Ӧ�����Է�Ӧ�ﵽƽ������CO���൱���ں��º�ѹ�����´�ƽ����ּ�ѹ��ƽ�����ƣ�CO��ת������ߣ�ƽ���������������ͣ���ȷ��D�����ʹ�ϵδ˵�������棬�����ж��Ƿ��Ѵ�ƽ�⣬����
��2����֪��������Ӧ�ֱ��â٢ڢ۱�ʾ�����ø�˹���ɿɵã�SO2��g��+2CO��g���TS��s��+2CO2��g�����ɡ��١�2+�ڡ�2-�۵õ������H=-��2Q2-2Q1-Q3�� kJ?mol-1��2Q1-2Q2+Q3��kJ?mol-1
��3��700��ʱ��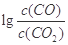 Խ����KԽС��˵����Ӧ���еij̶�С������������Խ�ѱ���ԭ������ͼ��Cr2O3��Ӧ��
Խ����KԽС��˵����Ӧ���еij̶�С������������Խ�ѱ���ԭ������ͼ��Cr2O3��Ӧ��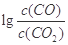 �������Cr2O3���ѱ���ԭ����ʱCr2O3��Ӧ��
�������Cr2O3���ѱ���ԭ����ʱCr2O3��Ӧ��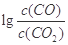 =4����c(CO2)/c(CO)=10-4�����Cr2O3��CO��Ӧ�Ļ�ѧ����ʽCr2O3+3CO
=4����c(CO2)/c(CO)=10-4�����Cr2O3��CO��Ӧ�Ļ�ѧ����ʽCr2O3+3CO 2Cr+3CO2���ɵ�K="[" c(CO2)/c(CO)]3=10-12��
2Cr+3CO2���ɵ�K="[" c(CO2)/c(CO)]3=10-12��
��4��ʯīI�缫��ͨ��NO2��Ϊ�����������ĵ缫��ӦΪ��NO2+NO3--e-=N2O5�����ݵ���ܷ�Ӧ4NO2+O2=2N2O5���ռ���20molN2O5������O2Ϊ10mol����״�������Ϊ224L��
���㣺���⿼�黯ѧƽ�⡢��˹���ɡ�ͼ��ķ�����ԭ���ԭ�������㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��9�֣���1����25�桢101kPa�£�1g����ȼ������CO2��Һ̬ˮʱ����55.6kJ�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ_________________________________________________��
��2���±��е����ݱ�ʾ�ƻ�1 mol��ѧ�������ĵ�����(�����ܣ���λΪkJ��mol��1)��
| ��ѧ�� | C��H | C��F | H��F | F��F |
| ���� | 414 | 489 | 565 | 158 |
 Al(OH)3(aq)
Al(OH)3(aq) Al3+(aq)+3OH-(aq)��ǰ��Ϊ�ܽ�ƽ�⣬����ǵ���ƽ�⣻
Al3+(aq)+3OH-(aq)��ǰ��Ϊ�ܽ�ƽ�⣬����ǵ���ƽ�⣻�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(4�֣���1mol��̬������ij�ֹ��ۼ���Ҫ���յ����������Ǹù��ۼ��ļ��ܡ��±���ijЩ���ۼ��ļ��ܣ�
| ���ۼ� | H-H | O=O | H-O |
| ����/kJ ��mol-1 | 436 | 498 | X |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(10��)��ѧ���������кܶ��Ӧ�ã�����������ڿ�������������ˮ��������ҵ���ﴦ������ΪƯ���ȣ�������(Si3N4)��һ�������մɲ��ϣ����нϸߵ�Ӳ�������¡�
��1���������������������ҿ������������е��ʷ�Ӧ����֪��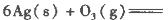
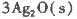 ��Ӧ����3 mol Ag2O(s)ʱ�ų�������Ϊ
��Ӧ����3 mol Ag2O(s)ʱ�ų�������Ϊ
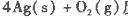 ��Ӧ����4 mol Ag(s)ʱ���յ�����Ϊ62��2 kJ���Ը�����������ж�O3ת��ΪO2��________������ȡ������ȡ�����Ӧ��
��Ӧ����4 mol Ag(s)ʱ���յ�����Ϊ62��2 kJ���Ը�����������ж�O3ת��ΪO2��________������ȡ������ȡ�����Ӧ��
��2��������()����ʯӢ�뽹̿�ڸ��µ���������ͨ�����·�Ӧ�Ƶã�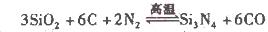
��VL���ܱ������н��з�Ӧ��ʵ���������±�: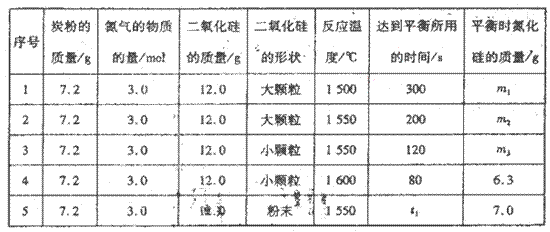
��ʵ��l��ʵ��2������________�Է�Ӧ������Ӱ�죬��ͬһ�����о���ʵ�黹��һ����________����ʵ����ţ�����ʵ�黹�о���_______�Է�Ӧ���ʵ�Ӱ�졣��
��ʵ��5�У�t1________(�>������<����=��)120��ƽ��ʱ�����������ת����Ϊ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(15��)
������AX3�͵���X2��һ�������·�Ӧ�����ɻ�����AX5���ش��������⣺
��1����֪AX3���۵�ͷе�ֱ�Ϊ��93.6 ���76 �棬AX5���۵�Ϊ167 �档����ʱAX3������X2��Ӧ����lmol AX5���ų�����123.8 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2����ӦAX3(g)��X2(g) AX5(g)���ݻ�Ϊ10 L���ܱ������н��С���ʼʱAX3��X2��Ϊ0.2 mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��
AX5(g)���ݻ�Ϊ10 L���ܱ������н��С���ʼʱAX3��X2��Ϊ0.2 mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��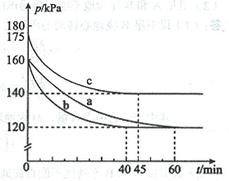
����ʽ����ʵ��a�ӷ�Ӧ��ʼ���ﵽƽ��ʱ�ķ�Ӧ���� v(AX5)�� ��
��ͼ��3��ʵ��ӷ�Ӧ��ʼ���ﵽƽ��ʱ�ķ�Ӧ����v(AX5)�ɴ�С�Ĵ���Ϊ (��ʵ�����)����ʵ��a��ȣ���������ı��ʵ���������ж������ǣ�b ��
c ��
����p0��ʾ��ʼʱ��ѹǿ��p��ʾƽ��ʱ��ѹǿ������ʾAX3��ƽ��ת���ʣ�����ı���ʽΪ
��ʵ��a��c��ƽ��ת���ʣ���aΪ ����cΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣������ǻ��������ĺ��ģ���������Ļ�������������ô����ա�
�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ[��Ӧ��O2(g)��������H2O(g)��ȥ]�����д��������£�CH3OH��O2��Ӧ��Ҫ���� ���CO��CO2��HCHO������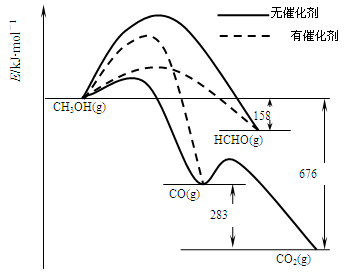
��2HCHO(g)��O2(g)��2CO(g)��2H2O(g)
��H�� ��
����ϡ������£�HCHO����ͨ����Ӧ���ɷ���ʽΪC3H6O3�Ļ�״���ۼ�ȩ���ӣ��������ͬ��ԭ�ӵĻ�ѧ��������ͬ��д�����ۼ�ȩ�Ľṹ��ʽ�� ��
�ܼ״���ȡ��ȩ����Ag������������AgCl��Ӱ��Ag�����Ļ��ԣ��ð�ˮ�����ܽ��ȥ���е�AgCl��д���÷�Ӧ�����ӷ���ʽ�� ��
��һ����ͭ�����������������������̣�
����ͭ����������ɹ�ҵβ����SO2�IJ��ִ���������������ӦΪ��
2SO2��2n Cu��(n��1)O2��(2��2 n) H2O��2n CuSO4��(2��2n) H2SO4
�ӻ��������ĽǶȿ��������������Ϊ ��ÿ���ձ�״����11.2L SO2����SO2��ԭ��O2������Ϊ
g��
��������ͼ��ʾ�绯ѧװ��������һ����SO2�������Cu��������д��װ������������Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����( COCl2)�����ϡ��Ƹ��ҩ�ȹ�ҵ����������;����ҵ�ϲ��ø�����CO��C12�ڻ���̿���ºϳɡ�
��1��ʵ�����п����ȷ�(CHC13)��˫��ˮֱ�ӷ�Ӧ�Ʊ��������䷴Ӧ�Ļ�ѧ����ʽΪ ��
��2����ҵ��������Ȼ��(��Ҫ�ɷ�ΪCH4)��CO2���и��������Ʊ�CO����֪CH4��H2��CO��ȼ����(��H)�ֱ�Ϊ?890.3kJ?mol?1��?285. 8 kJ?mol?1��?283.0 kJ?mol?1����1molCH4��CO2��Ӧ���Ȼ�ѧ����ʽ��
��3��COCl2�ķֽⷴӦΪCOCl2(g)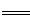 Cl2(g)��CO(g) ��H=��108kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͬ��ʾ(��10min��14min��COCl2Ũ�ȱ仯����δʾ��)��
Cl2(g)��CO(g) ��H=��108kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͬ��ʾ(��10min��14min��COCl2Ũ�ȱ仯����δʾ��)��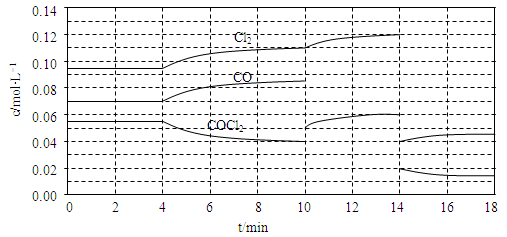
�ٱȽϵ�2 min��Ӧ�¶�T��2�����8min��Ӧ�¶�T��8���ĸߵͣ�T��2�� ____ T��8��(�<������>����=��)
�ڱȽϷ�Ӧ��COCl2��5?6min��15?16 minʱƽ����Ӧ���ʵĴ�С��v(5?6)
v(15?16)(�<������>����=��)��ԭ���� ��
�ۼ��㷴Ӧ�ڵ�8 minʱ��ƽ�ⳣ��K= �����г�������̣����������λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ú������Һ�����ִ���Դ��ҵ���ص㿼�ǵ���Դ�ۺ����÷������������������Ϊ��ú����ˮú��������ǰ�Ƚ����е�Һ������Ϊ��ú����CH3OH��
(1)��֪��CO2(g)��3H2(g)=CH3OH(g)��H2O(g)����H1
2CO(g)��O2(g)=2CO2(g)����H2
2H2(g)��O2(g)=2H2O(g)����H3
��ӦCO(g)��2H2(g)=CH3OH(g)�Ħ�H��______��
(2)��ͼ�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߡ�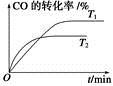
��T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1________K2(�����������������)��
����CO�ϳɼ״�ʱ��CO��250 �桢300 �桢350 ���´ﵽƽ��ʱת������ѹǿ�Ĺ�ϵ��������ͼ��ʾ��������c����ʾ���¶�Ϊ________ �档ʵ����������������250 �桢1.3��104 kPa���ң�ѡ���ѹǿ��������____________��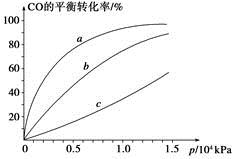
�������йظ÷�Ӧ��˵����ȷ����________(�����)��
A�����¡����������£��������ڵ�ѹǿ�������仯������淴Ӧ�ﵽƽ��
B��һ�������£�H2������������CO���������ʵ�2��ʱ�����淴Ӧ�ﵽƽ��
C��ʹ�ú��ʵĴ��������̴ﵽƽ���ʱ�䲢���CH3OH�IJ���
D��ij�¶��£���2 mol CO��6 mol H2����2 L�ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)��0.2 mol��L��1����CO��ת����Ϊ80%
(3)һ���¶��£���2 L�̶�������ܱ������м���1 mol CH3OH(g)��������Ӧ��CH3OH(g) CO(g)��2H2(g)��H2�����ʵ�����ʱ��仯��������ͼ��ʾ��
CO(g)��2H2(g)��H2�����ʵ�����ʱ��仯��������ͼ��ʾ��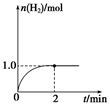
0��2 min�ڵ�ƽ����Ӧ����v(CH3OH)��__________�����¶��£���ӦCO(g)��2H2(g) CH3OH(g)��ƽ�ⳣ��K��__________����ͬ�¶��£�����ʼʱ����CH3OH(g)�����ʵ�����ԭ����2������__________(�����)��ԭ����2����
CH3OH(g)��ƽ�ⳣ��K��__________����ͬ�¶��£�����ʼʱ����CH3OH(g)�����ʵ�����ԭ����2������__________(�����)��ԭ����2����
A��ƽ�ⳣ�� B��CH3OH��ƽ��Ũ��
C���ﵽƽ���ʱ�� D��ƽ��ʱ������ܶ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com