
如图,在锥形瓶中按①②③④的顺序依次加入试剂后,立刻离开。可以观察到,大量的蓝色泡沫成柱状冲出锥形瓶,然后有白色泡沫迅速从锥形瓶口逸出,飞舞盘旋,并有大量水蒸气冒出。用手触摸锥形瓶,感觉比较烫。
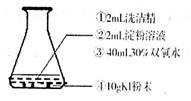
(1)开始冲出的泡沫呈蓝色,说明上述反应中生成了单质碘。试写出KI与H2O2反应生成碘的离子方程式 。
(2)已知1mol液态H2O2分解生成液态水和氧气,放出98.64kJ的热量。写出该反应的热化学方程式 。
(3)上述实验中KI粉末用KMnO4粉末代替,也可产生类似现象。在H2O2分别与这两种物质反应时,表现的性质有什么不同? 。
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
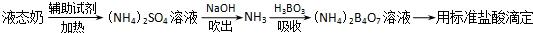
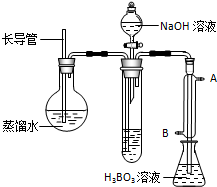
| 编号 | 样品和辅助试剂 | 消耗盐酸体积 |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45mL |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55mL |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50mL |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
为测定过氧化氢溶液的浓度,小明将一定量的过氧化氢溶液加入如图1的锥形瓶中,再加入少量二氧化锰,待反应完成后,称量锥形瓶和剩余物质的总质量。

(图1) (图2) (图3)
小明进行了四次实验,结果如下表:
| 序号 | 锥形瓶质量(g) | 过氧化氢溶液体积(mL) | 二氧化锰质量(g) | 反应完成后锥形瓶和剩余物质总质量(g) |
| 1 | 80.0 | 100.0 | 1.6 | 180.2 |
| 2 | 80.0 | 100.0 | 1.6 | 179.8 |
| 3 | 80.0 | 100.0 | 1.6 | 180.0 |
| 4 | 80.0 | 100.0 | 1.6 | 182.6 |
请回答下列问题:(假设过氧化氢溶液的密度为1 g •cm-3,实验在标准状况下进行)
(1)写出上述反应的化学方程式 ;
(2)若以上表中的数据计算,该过氧化氢溶液的物质的量浓度是 ;
(3)若用图2装置代替图1中的锥形瓶进行实验,结果将更准确,其理由是 ;
(4)若用图3装置代替图2进行实验,结果将更加准确,其理由是 ;
(5)若过氧化氢溶液的浓度约为1mol •L-1,取20.0 mL该溶液按图3方案进行实验,则该实验应选用的量筒规格是( );
A.1000 mL B. 500 mL C. 250 mL D. 100 mL
(6)有人认为上述三个方案均不够好,可以采用滴定的方法进行测定,其反应原理为:
2KMnO4+5H2O2+3H2SO4==K2SO4+2MnSO4+5O2↑+8H2O
若过氧化氢溶液的浓度约为1mol •L-1,取10.0 mL,用0.5000 mol•L-1酸化的高锰酸钾溶液进行滴定。则:
①滴定时,盛装高锰酸钾溶液应选用 (填“酸式”或“碱式”)滴定管;
②判断到达滴定终点的现象是 ;
③实验时,需要记录的数据有 ;
④消耗的酸化高锰酸钾溶液的体积约为 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(08年厦门市适应性考试)
为测定过氧化氢溶液的浓度,小明将一定量的过氧化氢溶液加入如图1的锥形瓶中,再加入少量二氧化锰,待反应完成后,称量锥形瓶和剩余物质的总质量。

(图1) (图2) (图3)
小明进行了四次实验,结果如下表:
序号 | 锥形瓶质量(g) | 过氧化氢溶液体积(mL) | 二氧化锰质量(g) | 反应完成后锥形瓶和剩余物质总质量(g) |
1 | 80.0 | 100.0 | 1.6 | 180.2 |
2 | 80.0 | 100.0 | 1.6 | 179.8 |
3 | 80.0 | 100.0 | 1.6 | 180.0 |
4 | 80.0 | 100.0 | 1.6 | 182.6 |
请回答下列问题:(假设过氧化氢溶液的密度为1 g •cm-3,实验在标准状况下进行)
(1)写出上述反应的化学方程式 ;
(2)若以上表中的数据计算,该过氧化氢溶液的物质的量浓度是 ;
(3)若用图2装置代替图1中的锥形瓶进行实验,结果将更准确,其理由是 ;
(4)若用图3装置代替图2进行实验,结果将更加准确,其理由是 ;
(5)若过氧化氢溶液的浓度约为1mol •L-1,取20.0 mL该溶液按图3方案进行实验,则该实验应选用的量筒规格是 ( );
A.1000 mL B. 500 mL C. 250 mL D. 100 mL
(6)有人认为上述三个方案均不够好,可以采用滴定的方法进行测定,其反应原理为:
2KMnO4+5H2O2+3H2SO4==K2SO4+2MnSO4+5O2↑+8H2O
若过氧化氢溶液的浓度约为1mol •L-1,取10.0 mL,用0.5000 mol•L-1酸化的高锰酸钾溶液进行滴定。则:
①滴定时,盛装高锰酸钾溶液应选用 (填“酸式”或“碱式”)滴定管;
②判断到达滴定终点的现象是 ;
③实验时,需要记录的数据有 ;
④消耗的酸化高锰酸钾溶液的体积约为 mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com