
【题目】短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+ 电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题:
(1)M元素位于周期表中的第________ 周期________ 族.
(2)Z元素的符号是 ________ ,其在自然界中常见的二元化合物是________ (写化学式) .
(3)X与M的单质在高温下反应的化学方程式为________,产物分子为直线形,其化学键属___ 共价键(填“极性”或“非极性”).
(4)四种元素中的________(写名称) 可用于航空航天合金材料的制备,其单质与稀盐酸反应的化学方程式为________________________ .
【答案】三 VIA Si SiO2 C+2S ![]() CS2 极性 镁 Mg+2HCl═MgCl2+H2↑
CS2 极性 镁 Mg+2HCl═MgCl2+H2↑
【解析】
短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,则X是C元素;Y2+电子层结构与氖相同,则Y是Mg元素;Z的质子数为偶数,室温下M单质为淡黄色固体,则Z是Si元素;M是S元素。
(1)M元素是S,核外电子排布是2、8、6,所以位于周期表中的第三周期、VIA族;
(2)Z元素是Si元素,其在自然界中常见的二元化合物是SiO2;
(3)X与M的单质在高温下反应产生CS2,该反应的化学方程式为C+2S ![]() CS2,产物分子为直线形,结构与CO2类似,由于是不同元素的原子形成的共价键,所以其化学键属于极性共价键;
CS2,产物分子为直线形,结构与CO2类似,由于是不同元素的原子形成的共价键,所以其化学键属于极性共价键;
(4)四种元素中只有Mg是金属元素,密度比较小,制成的合金硬度大,所以可用于航空航天合金材料的制备,该金属是比较活泼的金属,可以与盐酸发生置换反应产生氢气,其单质与稀盐酸反应的化学方程式为Mg+2HCl═MgCl2+H2↑。


科目:高中化学 来源: 题型:
【题目】已知 ![]() (x)、
(x)、![]() (y)、
(y)、![]() (z) 互为同分异构体,下列说法正确的是
(z) 互为同分异构体,下列说法正确的是
A. z的二氯代物有4种
B. x 和y 的所有原子均可能处于同一平面
C. 1分子y与1分子Br2 的加成产物有3 种(不考虑立体异构)
D. x、y、z 均可使溴的四氯化碳溶液因发生加成反应而褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了图中的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置略去)。
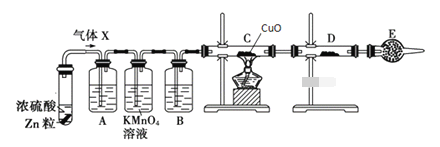
试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为__________。
(2)乙同学认为还可能产生氢气的理由是__________。
(3)A中加入的试剂可能是______,作用是__________;B中加入的试剂可能是__________,作用是_______;E中加入的试剂可能是__________,作用是__________。
(4)可以证明气体X中含有氢气的实验现象:C中__________,D中__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组查阅资料加。大多数硝酸盐不稳定。受热易分解,分解产物与金属活动顺序有关)了探究硝酸铁分解产物。他们进行如下探究:
(一)探究气体产物
[提出假设]
他们对气体产物提出如下猜想:
猜想1:气体为NO2
猜想2:气体为NO和O2
猜想3:气体为NO和NO2
清想4:气体为NO2和O2
猜想5:气体为NO
(1)他们经过讨论,认为猜想2不成立。理由是_______;根据氧化还原反应原理,不成立的猜想还有__________
[查阅资料]
①几种气体熔点。沸点如下:
气体 | NO | NO2 | O2 |
熔点/℃ | -163.6 | -11.2 | |
沸点/℃ | -151 | 21.1 | -183 |
②2NO2(g) ![]() N2O4(g)(无色) ΔH<0
N2O4(g)(无色) ΔH<0
[设计实验]
加热装置省略(冰盐冷却剂温度约为-5℃)

取一定量无水硝酸铁粉术进行实验,实验结果: A中U型管收集到少量液体物质;B中排水法收集一部分气体
(2)本实验的橡胶寨、导管接口处都用锡箔纸包裹,其目的是___________
(3)实验完毕,取出U型管,打开塞子。观察到有棕色气体产生,则U型管内的气体是_____
向U型管加入_____能吸收该物质。避免污染环境。
(4)检验B瓶收集气体为氧气的操作方法是__________
(二)探究固体成分
分析固体中铁元素价态,可能有种情况:①+2价②+3价③+2价和+3价。
为了探究固体中铁元素价态。甲、乙同学设计如下方案:
步骤 | 现象 | |
甲 | 取少量样品于试管,加入适量稀硫酸使固体完全溶解,再滴加酸性高锰酸钾溶液 | 溶液无明显颜色变化 |
乙 | 取少量样品于试管,加入稀盐酸使固体完全溶解,滴加KSCN溶液 | 溶液变红色 |
(5)上述实验,不能确定固体成分的实验是______(填“甲”或“乙”);根据上迷实验结论。写出硝酸铁分解反应的化学方程式______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了进一步改善北京地区的环境质量,下列做法不正确的是
A.推广使用无磷洗衣粉
B.使用清洁燃料的公交车
C.减少含硫化石燃料的大量燃烧
D.使用不易降解的一次性塑料餐具
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A. 加入催化剂可加快该反应的速率,从而提高SO2的转化率
B. 增大反应体系的压强,反应速率一定增大
C. 该反应是放热反应,故温度越低,对提高SO3的日产量越有利
D. 在2min时间内,SO2的浓度由6 mol/L变为3 mol/L,则在相同时间段内,SO3(g)生成的平均速率为1.5 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在2L密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图。下列叙述中正确的是( )
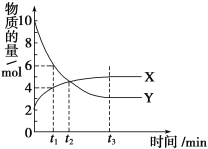
A. 反应的化学方程式为3X(g)![]() 7Y(g)
7Y(g)
B. t1时,Y的浓度是X浓度的1.5倍
C. t2时,正、逆反应速率相等
D. 0到t1时间段内,Y的平均反应速率为4/t1mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6mol X气体和0.4mol Y气体混合于2L容器中,发生反应:3X(g)+Y(g)== nZ(g)+2W(g),5min末已生成0.2mol W,若测知以Z浓度变化来表示的平均速率为0.03mol·L﹣1·min﹣1,计算:
(1)n的值为____;
(2)前5min内用X表示的反应速率_____;
(3)5min末Y的浓度_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下的六份溶液:①0.01molL﹣1 CH3COOH溶液;②0.01molL﹣1 HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01molL﹣1 CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01molL﹣1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液.
(1)其中水的电离程度最大的是__________(填序号,下同),水的电离程度相同的是_____________________.
(2)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②_____③(填“>”“<”或“=“).
(3)将六份溶液同等稀释10倍后,溶液的pH:①_____②,③_____④,⑤_____⑥(填“>”“<”或“=“).
(4)将①④混合,若有c(CH3COO﹣)>c(H+),则混合溶液可能呈___________(填序号).
A.酸性 B.碱性 C.中性.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com