
已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为 Y kJ/mol,则1 mol C与O2反应生成CO的反应热ΔH为____________
Y kJ/mol,则1 mol C与O2反应生成CO的反应热ΔH为____________
A.-Y kJ/mol B.-(10X-Y) kJ/mol
C.-(5X-0.5Y) kJ/mol D.+(10X-Y) kJ/mol
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学业水平测试化学卷(解析版) 题型:选择题
室内空气污染的主要来源之一是现代人的生活中使用的化工产品,如泡沫绝缘材料的办公用品、化纤地毯及书报、油漆等不同程度地释放出气体。该气体可能是( )
A.甲醛 B.甲烷 C一氧化碳 D.二氧化碳
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高一上学期期中联考化学试卷(解析版) 题型:计算题
l00mL稀H2S04和稀HC1的混合溶液中,部分离子的浓度关系如图所示,
(1)原混合液中H2SO4的物质的量 浓度 mol/L:
浓度 mol/L:
(2)向其中加入8.55g Ba(OH)2粉末,充分反应后,所得溶液中OH一的物质的量。(假设反应前后溶液体积不变,要求写出计算过程)。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
常温常压下,下列各组离子在指定溶液中能大量共存的是
A.c(Fe3+)=0.1 mol/L溶液中:Na+、NH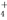 、SCN-、SO
、SCN-、SO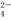
B.能溶解CaCO3的溶液中:Fe3+、Ca2+、Cl-、NO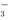
C.由水电离出的c(H+)=1×10-2mol/L的溶液中:Na+、Ba2+、HCO 、Cl-
、Cl-
D.强碱性溶液中:K+、Na+、ClO-、I-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:填空题
SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:
2SO2+O2 2SO3
2SO3  ΔH<0。
ΔH<0。
请回答下列问题:
(1)判断该反应达到平衡状态的标志是_____________(填字母)。
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
(2)当该 反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是_____________(填字母)。
反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是_____________(填字母)。
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程)。
①平衡常数K=____________________;
②平衡时,SO2的转化率α(SO2)=____________________。
(4)SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3。已知NaHSO3溶液同时存在以下两种平衡:①HSO
 SO
SO +H+,②HSO
+H+,②HSO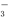 +H2O
+H2O H2SO3+OH-;常温下,0.1 mol/L NaH
H2SO3+OH-;常温下,0.1 mol/L NaH SO3溶液的pH<7,则该溶液中c(H2SO3)______________c(SO
SO3溶液的pH<7,则该溶液中c(H2SO3)______________c(SO )(填“>”、“=”或“<”)。
)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
常温下,pH=12的NaOH溶液与pH=1的HCl溶液按一定比例混合,所得溶液pH=2,则NaOH溶液与HCl溶液的体积比为
A.9∶2 B.2∶9 C.1∶9 D.10∶1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
某溶液可能含有Cl—、SO42—、CO32—、HCO3—、NH4+、Fe3+、Ba2+和K+。取该溶液100mL,加入过量NaOH溶液加热,得到0.02mol气体,同时产生1.97g白色沉淀;向上述滤液中加足量BaCl2溶液,也得到1.97g沉淀。由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl—)≥0.2mol/L
C.SO42—、NH4+一定存在,HCO3—可能不存在
D.Fe3+一定不存在,HCO3—、K+可能存在
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省郏县一高、叶县二高等五校高二上期中化学卷(解析版) 题型:填空题
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。
(3)能说明该反应达到化学平衡状态的是 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为 ℃。
(5)830℃时,在1L密闭容器中分别投入lmolH2和1molCO2反应达到化学平街时,CO2的转化率为 保持温度不变.在平衡体系中再充入1molH2和1 molCO2重新达到化学平衡时,CO2 的平衡转化率 (填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com