
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③④⑤ |
分析 钢铁生锈的过程是金属铁发生了吸氧腐蚀的原电池原理,铁为负极,发生失电子的氧化反应,正极上是氧气得电子发生还原反应,氢氧化亚铁易被氧气氧化为氢氧化铁,氢氧化铁失水即形成铁锈.
解答 解:钢铁生锈的过程是金属铁发生了吸氧腐蚀(或是析氢腐蚀)的原电池原理,铁为负极,发生失电子的氧化反应,Fe-2e-=Fe2+,正极上是氧气得电子发生还原反应,2H2O+O2+4e-=4OH-,O2被还原,或是在酸性环境下,氢离子得电子的过程,会产生氢气,氢氧化亚铁易被氧气氧化为氢氧化铁,4Fe(OH)2+O2+2H2O=4Fe(OH)3,Fe由+2价转为+3价,最后Fe(OH)3失水形成Fe2O3•xH2O,即为铁锈的成分;杂质碳是正极材料不参与反应;所以可能发生的是①②③④;
故选C.
点评 本题考查了钢铁的吸氧腐蚀和析氢腐蚀,注意根据原电池原理分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 三氧化二铁溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 铝与氢氧化钠溶液反应:2AI+2OH-═2 AIO2-+H2↑ | |
| D. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-29 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 纯净物 X、Y、Z 转化关系如右图所示,下列判断不正确的是( )
纯净物 X、Y、Z 转化关系如右图所示,下列判断不正确的是( )| A. | X 可能是金属铜 | B. | Y 可能是氢气 | ||
| C. | Z 不可能是氯化钠 | D. | Z 可能是三氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
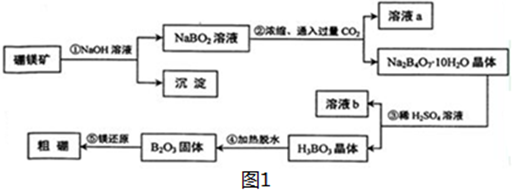
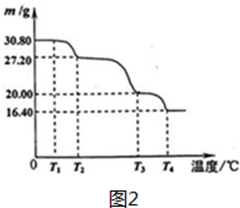
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铜与硝酸银溶液反应:Cu+2Ag+═2Ag+Cu2+ | |
| C. | 铁溶于稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com