
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是
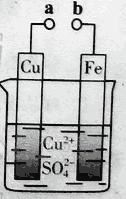
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
![]()
下列说法中不正确的是( )
A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C. B和Cl2的反应是氧化还原反应
D. 当X是强酸时,C在常温下是气态单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作所得出的现象和结论均正确的是( )
实验操作 | 实现现象 | 结论 | |
A | 向某溶液中先滴加氯水,再滴加少量KSCN溶液 | 溶液变成血红色 | 该溶液中有 |
B | 将石蜡油气化后,使气体流经碎瓷片,将生成的气体通入酸性高锰酸钾溶液 | 溶液紫红色褪去 | 碎瓷片的主要作用是使石蜡油受热均匀 |
C | 向 | 有砖红色沉淀生成 | Ksp: |
D | 将变黑的银器放入装满食盐水的铝盆中,二者直接接触 | 银器恢复往日光泽 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠是无色透明的晶体,易溶于水,其水溶液显碱性。在漂白工业中用作“脱氯剂”,常用黄铁矿(主要成分是![]() )经以下流程来制备硫代硫酸钠
)经以下流程来制备硫代硫酸钠
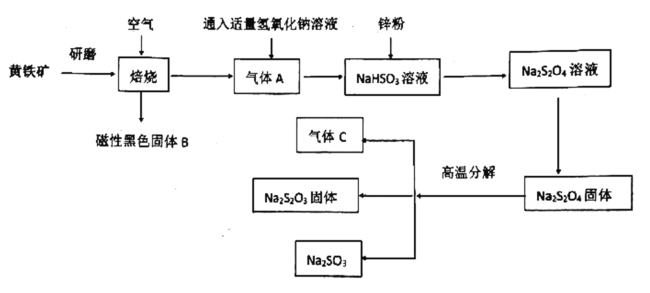
已知:气体C可以使品红溶液褪色
(1)研磨的目的是:____________,磁性黑色固体B的化学式为:________。
(2)尾气C能否用氢氧化钙溶液吸收:________(填“能”或“不能”),原因是:
________________。
(3)写出![]() 固体高温分解反应方程式:__________________________。
固体高温分解反应方程式:__________________________。
(4)![]() 溶液与盐酸不能稳定存在,用离子方程式解释不能存在的原因:
溶液与盐酸不能稳定存在,用离子方程式解释不能存在的原因:
____________________。
(5)请用“<”符号表示出亚硫酸氢钠溶液中的各离子浓度大小关系:____________。
(6)硫代硫酸钠在漂白工业中用作“脱氯剂”,标准状况下当消耗31.6g硫代硫酸钠时吸收氯气的积为:________L。
(7)已知![]() 溶液中
溶液中![]() ,求
,求![]() 的比值________(已知:
的比值________(已知:![]() 溶液的一级电离常数为
溶液的一级电离常数为![]() ,二级电离常数为
,二级电离常数为![]() ,水的电离常数为
,水的电离常数为![]() ,请用含有
,请用含有![]() 、
、![]() 、
、![]() 、b的式子表示)。
、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示。
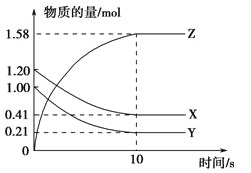
(1)从反应开始到10 s,用Z表示的反应速率为____。X的物质的量浓度减少了___,Y的转化率为_____。
(2)该反应的化学方程式为____。
(3)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是_____。

A.t1时刻,增大了X的浓度 B.t1时刻,缩小了容器体积
C.t1时刻,升高了体系温度 D.t1时刻,使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
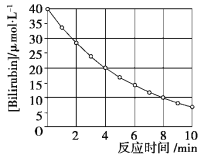
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种航天器能量储存系统原理示意图。下列说法正确的是
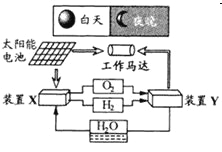
A. 该系统中只存在3种形式的能量转化
B. 装置Y中负极的电极反应式为:![]()
C. 装置X能实现燃料电池的燃料和氧化剂再生
D. 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从废旧锂离子二次电池(主要成分为![]() ,还含有少量石墨和镀镍金属钢壳、铝箔以及钙等杂质)中回收钴和锂的工艺流程如下:
,还含有少量石墨和镀镍金属钢壳、铝箔以及钙等杂质)中回收钴和锂的工艺流程如下:
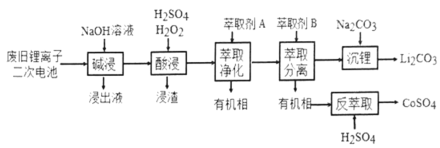
回答下列问题:
(1)“碱浸”目的是___________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为:_____________。浸渣含有的主要成分是_________。
发生反应的离子方程式为:_____________。浸渣含有的主要成分是_________。
(3)“萃取净化”除去的杂质离子有![]() 外,还有__________。
外,还有__________。
(4)“萃取分离”中钴、锂萃取率与平衡pH关系如图所示,pH一般选择5左右,理由是______________。

(5)“沉锂”中![]() 溶解度随温度变化曲线如下图所示:
溶解度随温度变化曲线如下图所示:
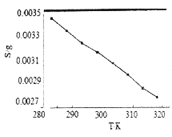
①根据平衡移动原理分析![]() 在水中溶解度随温度变化的原因____________________。
在水中溶解度随温度变化的原因____________________。
②为获得高纯![]() ,提纯操作依次为趁热过滤、________、烘干。
,提纯操作依次为趁热过滤、________、烘干。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为_______。利用反应6NO2+8NH3![]() 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______L。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______L。
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH1=﹣196.6 kJmol-1
2SO3(g) ΔH1=﹣196.6 kJmol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH2=﹣113.0kJmol-1
2NO2(g) ΔH2=﹣113.0kJmol-1
则反应NO2(g)+ SO2(g)![]() SO3(g)+NO(g)的ΔH=________kJmol-1。
SO3(g)+NO(g)的ΔH=________kJmol-1。
一定条件下,将2molNO2与2molSO2置于容积固定的恒温密闭容器中发生上述反应,下列能说明反应达到平衡状态的是__________(填字母)
a.混合气体密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1molSO3的同时生成1molNO2
该反应达平衡状态后,若再向该容器充入1molNO2与1molSO2,则SO2的转化率将_______(填“增大”“减小”或“不变”)。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g) ΔH=﹣a kJmol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为_______,正反应放出的热量为______。
CH3OH(g) ΔH=﹣a kJmol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为_______,正反应放出的热量为______。
(4)已知N2O4(g)![]() 2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是_______。
2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是_______。
A.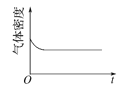 B.
B.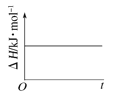 C.
C.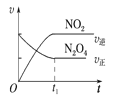 D.
D.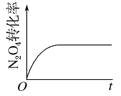
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com