
ij��ѧС�����Na2SO3 ������ʵ��̽����
��1���ڰ�ɫ��ΰ��a��b��c���������е���Na2SO3 ��Һ���ٷֱ�μ���ͼ��ʾ���Լ���
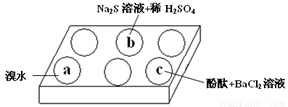
ʵ���������±���
|
��� |
ʵ������ |
|
a |
��ˮ��ɫ |
|
b |
��������ɫ���� |
|
c |
�����̪��Һ��죬�ټ���BaCl2��Һ����������Һ�ɫ��ȥ |
����ʵ��������з�����
�� a��ʵ������֤��Na2SO3���� �ԡ�
�� b�з�����Ӧ�����ӷ���ʽ�� ��
�� Ӧ�û�ѧƽ��ԭ������c�������û�ѧ���P�����ֱ����� ��
��2������NaOH ��Һ����SO2 �Ĺ����У������õ�Na2SO3��NaHSO3 �Ļ����Һ����ҺpH ��n(SO32-):n(HSO3-) �仯��ϵ���±���
|
n(SO3 2��)�� n(HSO3��) |
91��9 |
1��1 |
9��91 |
|
pH |
8.2 |
7.2 |
6.2 |
�� ������Һ��n(SO32-):n(HSO3-) =10:1 ʱ����Һ������Ũ�ȹ�ϵ��ȷ���� ������ĸ����
A��c(Na+) +c(H+) = 2c(SO32-) +c(HSO3-) + c(OH-)
B��c(Na+) > c(HSO3-) > c(SO32-) > c(OH-)>c(H+)
C��c(Na+) > c(SO32-) > c(HSO3-) > c(OH-)>c(H+)
�� ��n(SO32-):n(HSO3-) = 3:2����0.8 mol NaOH��Һ�����˱�״���µ�SO2 L��
��10�֣�
��1���ٻ�ԭ�� ��2�֣�
��SO32-+2S2-+6H+= 3S��+3 H2O ��2�֣�
����Na2SO3��Һ�У�SO32-ˮ���Լ��ԣ�SO32-+H2O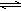 HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
��2����AC ��2�֣�
��11.2 ��2�֣�
��������
�����������1����SO2��Br2��2H2O=H2SO4��2HBr��SO2��S���ϼ����ߣ����������Ի�ԭ�ԣ��𰸣���ԭ�� ��2�֣�
�����������£�+4�۵�S��-2�۵�S��Ӧ������0�۵�S,���е���ɫ�������𰸣�SO32-+2S2-+6H+= 3S��+3 H2O ��2�֣�
��SO32�D����������ӣ�ˮ���ʼ��ԣ���Ba2��ˮ��ƽ�ⱻ�ƻ����𰸣���Na2SO3��Һ�У�SO32-ˮ���Լ��ԣ�SO32-+H2O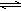 HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
��2����A��ȷ����Һ�д��ڵ���غ㣬B����ȷ��c(SO32-) > c(HSO3-)��C����ȷ��n(SO3 2��)�� n(HSO3��)= 91��9ʱ��pH=8.2����Һ�ʼ��ԣ�c(Na+) > c(SO32-) > c(HSO3-) > c(OH-)>c(H+)����ȷ���ʴ𰸣�AC ��2�֣�
����n(SO32-):n(HSO3-) = 3:2����0.8 mol NaOH��Һ�����˱�״���µ�SO2���������n(SO32-)=3x������Na�� �غ�ã�3x��2��2x=0.8mol,x=0.1mol,n(SO2)=0.5mol,v(SO2 )=0.5mol��22.4l��mol-1=11.2L,�𰸣�11.2 ��2�֣�
���㣺Ԫ�ؼ��仯���������뻯ѧʵ�顢��ѧ��Ӧԭ���ۺϡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡ����һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
(14��)ij�о���ѧϰС�齫һ��Ũ�ȵ�Na2 CO3 ��Һ����CuSO4 ��Һ�еõ���ɫ��������ͬѧ��Ϊ���߷�Ӧֻ����һ�ֳ���CuCO3 ����ͬѧ��Ϊ������ٽ�ˮ�⣬ֻ����һ�ֳ���Cu(OH)2 ����ͬѧ��Ϊ����CuCO3 ��Cu(OH)2���ֳ������۲�������֪��CuCO3 ��Cu(OH)2 �������ᾧˮ��
��.������ͬѧ�����⣬Na2 CO3 ��Һ��CuSO4 ��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��̽��������ɷ�ǰ���뽫��������Һ�з��벢��������������ٹ��ˡ���ϴ�ӡ��۸��
��.������ͼ��ʾװ�ã�ѡ���Ҫ���Լ�������̽��������ijɷ֡�
(1)��װ������˳��Ϊ ��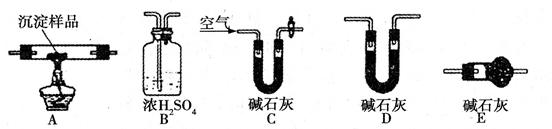
(2)װ��C����װ�Լ��������� ��
(3)��֤������������CuCO3 ��ʵ�������� ��
��.��CuCO3 ��Cu(OH)2���߶��У���ͨ��������ʾװ�ý��ж����������ⶨ����ɡ�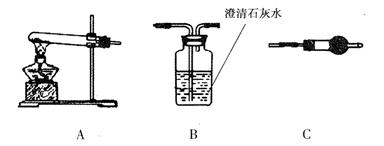
(1)װ��C�м�ʯ�ҵ������� ��ʵ�鿪ʼ��ʵ�����ʱ��Ҫͨ������Ŀ�������ʵ�����ʱͨ������������� ��
(2)��������Ʒ������Ϊm g��װ��B������������n g���������CuCO3����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
(14��)ij�о���ѧϰС�齫һ��Ũ�ȵ�Na2 CO3 ��Һ����CuSO4 ��Һ�еõ���ɫ��������ͬѧ��Ϊ���߷�Ӧֻ����һ�ֳ���CuCO3 ����ͬѧ��Ϊ������ٽ�ˮ�⣬ֻ����һ�ֳ���Cu(OH)2 ����ͬѧ��Ϊ����CuCO3 ��Cu(OH)2���ֳ������۲�������֪��CuCO3 ��Cu(OH)2 �������ᾧˮ��
��.������ͬѧ�����⣬Na2 CO3 ��Һ��CuSO4 ��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��̽��������ɷ�ǰ���뽫��������Һ�з��벢��������������ٹ��ˡ���ϴ�ӡ��۸��
��.������ͼ��ʾװ�ã�ѡ���Ҫ���Լ�������̽��������ijɷ֡�
(1)��װ������˳��Ϊ ��
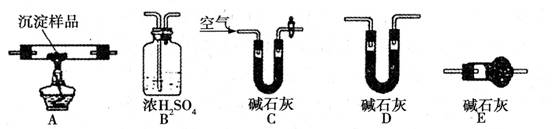
(2)װ��C����װ�Լ��������� ��
(3)��֤������������CuCO3 ��ʵ�������� ��
��.��CuCO3 ��Cu(OH)2���߶��У���ͨ��������ʾװ�ý��ж����������ⶨ����ɡ�

(1)װ��C�м�ʯ�ҵ������� ��ʵ�鿪ʼ��ʵ�����ʱ��Ҫͨ������Ŀ�������ʵ�����ʱͨ������������� ��
(2)��������Ʒ������Ϊm g��װ��B������������n g���������CuCO3����������Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com