
铜是应用较为广泛的有色金属。
(1)基态铜原子的价电子排布式为_____________。
(2)金属化合物Cu2Zn合金具有较高的熔点、较大的强度、硬度和耐磨度。则Cu2Zn合金的晶体类型是______。
(3)某含铜化合物的离子结构如图所示。

① 该离子中存在的作用力有__________。
a.离子键 b.共价键 c.配位键
d.氢键 e.范德华力
② 该离子中第二周期的非金属元素的第一电离能由大到小的顺序是______。
③ 该离子中N原子的杂化类型有_________。
(4)晶胞有两个基本要素:
① 原子坐标参数,表示晶胞内部各原子的相对位置,下图为铜与氧形成的某化合物晶胞,其中原子坐标参数A 为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为_____________。
,0),则D原子的坐标参数为_____________。
② 晶胞参数,描述晶胞的大小和形状,设晶胞的边长为apm,则O的配位数是_______。

科目:高中化学 来源:2016-2017学年宁夏孔德校区高一下学期第一次(3月)月考化学试卷(解析版) 题型:选择题
下列反应中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
查看答案和解析>>
科目:高中化学 来源:河北省唐山市2016-2017学年高二3月月考化学试卷 题型:选择题
使1mol 乙烯与氯气完全反应发生加成反应,后使该加成反应的产物与足量氯气在光照的条件下发生取代反应,则两个过程中消耗的氯气的总的物质的量是
A.3mol B.4mol C.5mol D.6mol
查看答案和解析>>
科目:高中化学 来源:2017届安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:简答题
2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、 硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图所示)可用于ⅢB族元素对应的离子萃取,如La2+、Sc2+。写出基态二价钪离子(Sc2+)核外电子排布式:__________。其中电子占据的轨道数为__________个。

(2)对叔丁基杯[4]芳烃由4个烃基构成杯底,其中条件氧原子的杂化方式为___________。烃基间的相互作用力为_______________。
(3)不同大小的杯芳烃能识别某些离子,如:N3-、SCN-等。根据等电子体原料判断N3-空间构型为______;一定条件下,SCN-与MnO2反应可得到(SCN)2。试写出(SCN)2 的结构式:_______________。
(4)已知C60分子结构和C60晶胞示意图(如图Ⅱ,图Ⅲ所示):
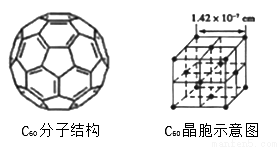
则一个C60分子中含有σ键个数为__________,与每个C60分子距离最近且相等的C60分子有_________个,C60晶体的密度为__________(计算结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:选择题
某种医药中间体X,其结构简式如下图。下列有关该化合物说法正确的是

A. X的分子式为C16H11O4
B. X分子中有3种不同的官能团
C. X分子中3个六元环可能处于同一平面
D. 即能发生酯化反应,又能发生水解反应
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三下学期模考4理科综合化学试卷(解析版) 题型:选择题
在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n)的取值范围是( )
A. n≥1 B. 1<n<2 C. 2≤n<4 D. n≥4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北京市怀柔区高一上学期期末考试化学试卷(解析版) 题型:推断题
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
(1)若A为H2S,D的水溶液能使湿润的蓝色石蕊试纸变红,B为刺激性气味气体,写出B→C转化的化学反应方程式:________________________________________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红:A的化学式为______,实验室制备气体A的化学反应方程式__________________________,A→B转化的化学方程式为_____________________________________________________。
(3)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则B是(填化学式)________, C可作为呼吸面具的填充剂,C与二氧化碳发生反应的化学方程式为________________________________,C与水发生反应的离子方程式为___________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北京市怀柔区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.1 mol任何气体的摩尔体积都约是22.4 L
B.标准状况时,体积均为22.4 L的O2与CO2含有相同的分子数
C.处于标准状况的两种气体,当体积均为22.4 L时的质量完全相同
D.标准状况时,2 mol任何物质的体积均约为44.8 L
查看答案和解析>>
科目:高中化学 来源:湖北省沙市2016-2017学年高二下学期第三次双周考化学试卷(A卷) 题型:填空题
钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如下表;
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述盐溶液中的阴离子,结合氢离子能力最强的是 ,根据表中数据,浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL0.1mol/L碳酸氢钠 ②100mL0.1mol/L碳酸钠两种溶液,溶液中水电离出的氢离子个数:
① ② (填“>”“=”“<”下同)。溶液中阴离子的物质的量浓度之和:① ②。
(3)碳酸氢钠是一种 (填“强”或“弱”)电解质;写出HCO3-水解的离子方程式: ,常温下,0.1mol/L碳酸氢钠溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为: 。
(4)实验室中常用氢氧化钠来进行洗气和提纯。
①当150mL1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为: 。
② 几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)3]
Ksp[Mg(OH)2] (填“>”“=”或“<”),要使0.2mol/L硫酸铜溶液中铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。
( Ksp[Cu(OH)2]=2×10-20mol2/L2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com