
下列反应中符合下图图象的是( )
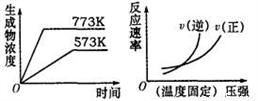
A. N2(g) +3H2(g) 2NH3(g) ;△H=—Q1kJ·mol—1(Q1>0)
2NH3(g) ;△H=—Q1kJ·mol—1(Q1>0)
B. 2SO3(g) 2SO2(g)+O2(g) ;△H=+Q2kJ·mol—1(Q2>0)
2SO2(g)+O2(g) ;△H=+Q2kJ·mol—1(Q2>0)
C. 4NH3(g)+5O2(g) 4NO(g)+6H2O(g);△H=—Q3kJ·mol—1(Q3>0)
4NO(g)+6H2O(g);△H=—Q3kJ·mol—1(Q3>0)
D. H2(g) +CO(g) C(s)+H2O(g); △H=+Q4kJ·mol—1(Q4>0)
C(s)+H2O(g); △H=+Q4kJ·mol—1(Q4>0)
科目:高中化学 来源:2017届江西省协作体高三下学期第一次联考理综化学试卷(解析版) 题型:填空题
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节.某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下
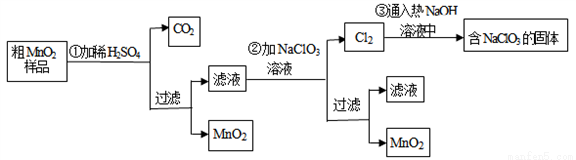
(1)第①步加稀H2SO4时,粗MnO2样品中的_____________(写化学式)转化为可溶性物质.
(2)第②步反应的离子方程式:_______________________
(3)流程中得到MnO2固体操作必需的玻璃仪器有玻璃棒、烧杯、_______________。
(4)已知第③步蒸发得到的固体中有NaClO3和NaOH,则一定还有含有_________(写化学式).其中用到Cl2的实验室制法的反应离子方程式:_______________________。
(5)若粗MnO2样品的质量为50.76g,第①步反应后,经过滤得到34.8g MnO2,并收集到0.896LCO2(标准状况下),则在第②步反应中至少需要____________ g NaClO3.[M (NaClO3)=106.5]
(6)第①步酸溶产生的CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2]。己知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s); ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CONH2)2(s)+H2O(g); ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高二上学期开学检测化学试卷(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是( )
A. 生成物总能量一定低于反应物总能量
B. 放热反应的反应速率总是大于吸热反应的反应速率
C. 根据盖斯定律,可计算某些难以直接测量的反应焓变
D. 同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件的ΔH不同
2HCl(g)在光照和点燃条件的ΔH不同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷(解析版) 题型:简答题
针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
活动一:查阅资料:NaNO2有毒,溶液显碱性,NaNO2有较强的氧化性和较弱的还原性。国家规定肉制品中NaNO2含量不能超过30 mg/kg。
(1)NaNO2溶液显碱性的原因是_____________________。(用离子方程式表达)
活动二:鉴别NaNO2与食盐
(2)可用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是_________。(填化学式)。
活动三:检测熟肉中NaNO2含量的变化
(3)分别从 1000 g刚煮熟的肉和 1000 g隔夜熟肉中提取NaNO2,配成溶液,再分别用0.00500 mol/L酸性高锰酸钾溶液滴定,刚煮熟的肉消耗12.00 mL,隔夜熟肉消耗16.00 mL。(提示:MnO4一转化为Mn2+,NO2一转化为NO3一)
① 在做该滴定实验时需要用到的实验仪器有___________
A.容量瓶 B.酸式滴定管 C.碱式滴定管
D.分液漏斗 E.锥形瓶 F. 烧瓶
② 滴定终点的判断依据为_________________ 。
③ 隔夜熟肉中NaNO2的含量是____________mg/kg (保留三位有效数字),该数据说明保存得当的隔夜熟肉_________(选填“能”或“不能” )食用。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A. 将过量SO2通入稀氨水中:SO2+NH3•H2O=HSO3﹣+NH4+
B. Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C. 大理石溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑
D. AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=[Al(OH)4]﹣+4NH4+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是( )
A. 用pH试纸测双氧水的pH
B. 用酸式滴定管量取20.00 mL酸性KMnO4溶液
C. 用托盘天平称取 5.85 g NaCl晶体
D. 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省马鞍山市高二上学期期末考试化学试卷(解析版) 题型:选择题
有关如图所示化合物的说法不正确的是:
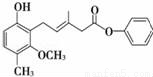
A. 该化合物既可以催化加氢,又可以在光照下与Cl2发生取代反应
B. 该化合物既可以与溴水反应,又可以使酸性KMnO4溶液褪色
C. 该化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2
D. 1 mol该化合物最多可以与3mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一上学期期末考试化学试卷(解析版) 题型:实验题
某难溶于水的化合物粉末中除含有碳粉外,还可能含有铁、铝的单质和它们的某一种氧化物。某校实验小组通过实验确定该混合物粉末的成分。
实验步骤:
①取m g固体粉末于一烧杯中,加入足量NaOH稀溶液,有气体放出,过滤得到固体A和无色溶液B;
②将①中所得固体A洗涤后分成两份。一份加入CuSO4溶液,无明显变化;另
一份加入足量稀硫酸,过滤得到固体C和棕黄色溶液D。
请回答下列问题:
(1)写出步骤①中发生反应的离子方程式____________________
(2)固体C的一种氧化物与过氧化钠发生反应的化学方程式为__________________。
(3)向棕黄色溶液D中加入铁粉,发生反应的离子方程式为_________________。
(4)由上述实验可以得出结论:混合物粉末中一定含有碳和________(填化学式,下同),含铁元素的物质可能是________或________。若要确定含铁元素的物质,还需要进一步实验,该实验方法为__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高一下学期开学检测化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A. 铁与稀硫酸反应:2Fe + 6H+ = 2Fe3﹢ +3H2↑
B. Al(OH) 3沉淀中滴加盐酸:Al(OH)3 + H﹢ = Al3﹢+H2O
C. 碳酸氢钠溶液中加入氢氧化钠:HCO3- + OH- = CO32- + H2O
D. 碳酸钙与稀硝酸反应:CO32- + 2H+= CO2↑ + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com