
(8分)下表是五种主族元素的结构特点及其元素、单质、化合物的性质。
元素 | 结构特点及元素、单质、化合物的性质 |
X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
W | 最外层电子排布(n+1)s n (n+1)p n-1 |
T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布 ;其单质的化学性质 (填“稳定”或“活泼”),该元素的非金属性 (填“强”或“弱”),证明其强弱的理由是 。
![]() (2)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反应的离子方程式: , 。
(2)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反应的离子方程式: , 。
![]() (3)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式 。
(3)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式 。
![]() (4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱。Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱。Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为
![]() A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3
 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | Z |
| 甲 | 乙 | 丙 |
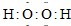
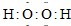
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:
下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:| 元素 | 有关信息 |
| A | 元素主要化合价为-2,原子半径为0.074n m |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102n m,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物的水化物,能按1:1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075n m,最高价氧化物的水化物与其氢化物组成一种盐X |




 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?闸北区二模)某同学在研究前l8号元素时发现,可以将它们按原子序数递增的顺序排成如右图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中O点代表氢元素.
(2012?闸北区二模)某同学在研究前l8号元素时发现,可以将它们按原子序数递增的顺序排成如右图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中O点代表氢元素.| 共价键 | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com