
次氯酸可用于杀菌消毒。已知25°C时:
①HClO(aq)+OH-(aq)= ClO-(aq)+ H2O(l) ΔH=-Q1kJ·mol-1
②H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ·mol-1
下列说法正确的是
A.在25°C时,次氯酸的电离方程式及热效应可表示为:
HClO(aq)=H+(aq)+ClO-(aq)ΔH=-(57.3+Q1)kJ·mol-1
B.将20ml 1mol/L HClO与10ml 1mol/L NaOH混合后的溶液,一定存在:
2C(H+)-2C(OH-)=C(ClO-)-C(HClO)
C.已知酸性H2SO3>HClO>HSO3-, 则向Na2SO3溶液中加入HClO的离子方程式为:SO32-+ HClO= HSO3-+ ClO-
D.已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:
C(Na+)> C(ClO-)> C(CH3COO-)> C(OH-)> C(H+)
B
【解析】
试题分析:A、根据盖斯定律,在25°C时,次氯酸的电离方程式及热效应可表示为: HClO(aq)=H+(aq)+ClO-(aq)ΔH=-(Q1—57.3)kJ·mol-1,错误;B、将20mL 1mol/L HClO与10mL 1mol/L NaOH混合后所得的溶液是等浓度的次氯酸和次氯酸钠的混合物,根据电荷守恒:c(H+)+c(Na+)=c(OH-)+c(ClO-),根据物料守恒:2c(Na+)=c(ClO-)+c(HClO),整理两个等式得到2c(H+)-2c(OH-)=c(ClO-)-c(HClO),正确;C、向Na2SO3溶液中加入HClO,次氯酸将亚硫酸钠氧化为硫酸钠,不会发生复分解反应,错误;D、等浓度CH3COONa和NaClO的混合液中,由于酸性CH3COOH>HClO,所以次氯酸根离子水解程度大与醋酸钠根离子,C(ClO-)<C(CH3COO-),溶液显碱性,所以C(Na+)>C(CH3COO-)>C(ClO-)>C(OH-)>C(H+),错误。
考点:本题考查反应热的大小比较、离子浓度比较、离子方程式书写。


科目:高中化学 来源:2013-2014安徽省高二(下)期末考试化学试卷(解析版) 题型:选择题
某醇与足量的金属钠反应,产生的氢气与醇的物质的量之比为1:1,则该醇可能是( )
A.甲醇 B.乙醇 C.乙二醇 D.丙三醇
查看答案和解析>>
科目:高中化学 来源:2013-2014安徽省、合肥六中第二学期期末联考高一化学试卷(解析版) 题型:选择题
下列除杂方法(括号内为杂质)操作正确的是( )
A.乙醇(水) 加新制的生石灰,过滤
B.乙烷(乙烯) 通过溴水溶液,洗气
C.溴苯(苯) 加水,振荡静置后分液
D.乙酸乙酯(乙酸) 加饱和NaHCO3溶液,振荡静置后蒸馏
查看答案和解析>>
科目:高中化学 来源:2013-2014安徽省合肥市高三第三次教学质量检测理综化学试卷(解析版) 题型:选择题
-定条件下,在体积为VL的密闭容器中发生如下反应 一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
A.若升高温度,反应混合气体密度不变时即达到新平衡状态
B.若增大B的浓度,△H减小
C.若使用适当催化剂,A的转化率增大
D.若增大压强,平衡向右移动,则m+n>p+q
查看答案和解析>>
科目:高中化学 来源:2013-2014宁夏银川市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)
第五主族的磷单质及其化合物在工业上有广泛应用。
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) 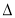 H
H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) △H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g) △H2
SiO2(s)+CaO(s)=CaSiO3(s) △H3
用△H1、△H2和△H3表示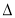 H,则
H,则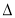 H= ;
H= ;
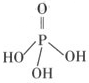
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两
个水分子产物,其结构式为 ,三聚
磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为 ;
(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍。
①化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a) Ni2+ + H2PO2-+ → Ni++ H2PO3-+
(b)6H2PO-2 +2H+ =2P+4H2PO3+3H2↑ 请在答题卡上写出并配平反应式(a);
请在答题卡上写出并配平反应式(a);
②利用①中反应可在塑料镀件表面沉积镍—磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
方法上的不同点: ;
原理上的不同点: ;
化学镀的优点: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014宁夏银川市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
有机化学在日常生活应用广泛,下列有关说法不正确的是
A.相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大
B.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
C.甲苯和Cl2光照下的反应与乙醇和乙酸的反应属于同一类型的反应
D.有芳香气味的C9H18O2在酸性条件下加热可水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有16种
查看答案和解析>>
科目:高中化学 来源:2013-2014宁夏高二下学期期末考试化学试卷(解析版) 题型:选择题
下列现象和应用与电子跃迁无关的是( )
A.激光 B.焰色反应 C.原子光谱 D.石墨导电
查看答案和解析>>
科目:高中化学 来源:2013-2014宁夏高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.CHCl3是正四面体形
B.H2O分子中氧原子为sp2杂化,其分子几何构型为V形
C.二氧化碳中碳原子为sp杂化,为直线形分子
D.NH 是三角锥形
是三角锥形
查看答案和解析>>
科目:高中化学 来源:2013-2014学年陕西省五校高三第三联考理综化学试卷(解析版) 题型:填空题
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:

部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,该反应的氧化剂为_____________。
(2)滤液中含钒的主要成分为______________(填化学式)。
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式____;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为___________、_________℃。

(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应方程式为:2VO2++H2C2O4+2H+=2VOn+ + 2CO2↑+ mH2O,其中n、m分别为______________、________ 。
(5)全钒液流电池的电解质溶液为VOSO4溶液,电池的工作原理为: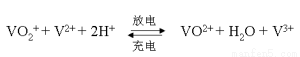
电池放电时正极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com