
(16分)铁及其化合物在生产、生活中应用广泛。
(1)一定条件下,Fe与CO2可发生反应:
2Fe(s)+3CO2(g) Fe2O3(s)+3CO(g)
Fe2O3(s)+3CO(g)
该反应的平衡常数(K ) 随温度(T ) 升高而增大。
①该反应的平衡常数K= ______。(填表达式)
②下列措施中,能使平衡时c(CO)/c(CO2) 增大的是 (填标号)。
| A.升高温度 | B.增大压强 |
| C.充入一定量CO | D.再加一些铁粉 |
(1)① (2分) ② A (2分)
(2分) ② A (2分)
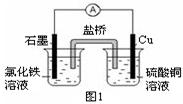
(2) 2Fe3+ + Cu = 2Fe2+ + Cu2+(2分)zxxk
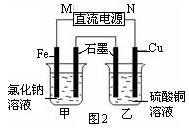
(3)① 正(2分), Fe - 2e-= Fe2+(2分)
② 2CuSO4+ 2H2O 2Cu + O2↑ + 2H2SO4 (3分) ③ 224(3分)
2Cu + O2↑ + 2H2SO4 (3分) ③ 224(3分)
解析试题分析:(1)①平衡常数只与气态物质的浓度有关,所以表达式中没有出现固体物质。②升高温度,平衡常数增大。(2)为原电池,反应为硫酸铜与氯化铁发生,先写出化学方程式,再把硫酸铜和氯化铁拆开。(3)①铁失电子,进入M,则M为正极。②反应为电解硫酸铜,产生铜单质和氧气。注意配平。③根据铜的物质的量为0.01mol,则转移的电子为0.02mol,根据电子得失守恒,所消耗的铁为0.02mol,而石墨上产生的气体为氯气,得到0.02mol电子,产生的气体为0.01mol,体积为224ml。
考点:化学反应平衡常数,原电池,电解池。
点评:本题最后一问比较新颖,将原电池和电解池连接在一起,解题关键在于抓住电子得失守恒。另外本题还综合了化学反应平衡常数的知识,综合性较大,是一道不错的题目,难度一般。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:阅读理解
 镁、铝、铁及其化合物在生产和生活中有广泛的应用.
镁、铝、铁及其化合物在生产和生活中有广泛的应用.| 实验序号 | I | II | III |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
| 0.12 |
| 28.12 |
| 0.12 |
| 28.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c3(CO) |
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c(CO) |
| c(CO2) |

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012届福建省莆田二中高三上学期期中考试化学试卷(带解析) 题型:填空题
硅、铝和铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)30Si原子的中子数为 ,Si的晶体类型为 。
(3)Al3+与Yn—的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是 。
(4)某焊药熔渣36.0g(含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体。则此熔渣中Al2O3的质量分数为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com