

①提出合理假设
假设1:只存在SO32-
假设2:既不存在SO32-也不存在ClO-
假设3:_____________
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
|
实验步骤 |
预期现象和结论 |
|
步骤1:取少量吸收液于试管中,滴加3 moL |
|
|
步骤2: |
|
|
步骤3: |
|
解析:(1) NaOH过量,故生成的是正盐:SO2+2NaOH =Na2SO3+H2O。
(2)S元素的价态从+4→+6,失去电子做表现还原性,故还原剂为Na2SO3。
(3)①很明显,假设3两种离子都存在。
②加入硫酸的试管,若存在SO32-、ClO-,分别生成了H2SO3和HClO;在A试管中滴加紫色石蕊试液,若先变红后退色,证明有ClO-,否则无;在B试管中滴加0.01mol L-1KMnO4溶液,若紫红色退去,证明有SO32-,否则无。
L-1KMnO4溶液,若紫红色退去,证明有SO32-,否则无。
答案:
(1) Na2SO3+H2O
(2) Na2SO3
(3) ①SO32-、ClO-都存在
②
|
实验步骤 |
预期现象和结论 |
|
步骤1:取少量吸收液于试管中,滴加3 moL |
|
|
步骤2:在A试管中滴加紫色石蕊试液 |
若先变红后退色,证明有ClO-,否则无 |
|
步骤3:在B试管中滴加0.01mol |
若紫红色退去,证明有SO32-,否则无 |


科目:高中化学 来源: 题型:
某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究(可供选用的实验仪器及试剂如下)。

(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3: 。
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a— (每组选用仪器和试剂限用一次)。
(3)根据(2)的连接顺序进行实验,填写相应现象。
| 假设方案编号 | 相应现象 |
| 假设1 | |
| 假设2 | |
| 假设3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究(可供选用的实验仪器及试剂如下)。
(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3: 。
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a— (每组选用仪器和试剂限用一次)。
(3)根据(2)的连接顺序进行实验,填写相应现象。
| 假设方案编号 | 相应现象 |
| 假设1 |
|
| 假设2 |
|
| 假设3 |
|
查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省合肥市高三第二次教学质量检测(二模)化学试卷(解析版) 题型:实验题
三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究。该小组同学查阅资料知,固体产物中铁元素不可能以三价形式存在,而盐只有K2CO3,产生的气体中含有CO、CO2。
请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
限选试剂:①蒸馏水②3%H2O2溶液③氧化铜④1.0mol/L盐酸⑤浓硫酸⑥1.0mol/LNaOH溶液⑦澄清石灰水⑧0.5 mol/LCuSO4溶液⑨2%KSCN溶液⑩苯酚溶液
I.若用一套连续实验装置检验气体产物中CO的存在,并验证检验过程中有CO2生成,应选用的试剂为(按先后顺序把所选试剂的标号填入空格内) 。
Ⅱ.探究固体产物中铁元素的存在形式。
(1)提出合理假设
假设1:只有Fe;
假设2:只有FeO;
假设3:
(2)设计实验方案并实验验证
步骤1:取适量固体产物于试管中,加入足量蒸馏水溶解,过滤分离出不溶固体。
步骤2:取少量上述不溶固体放人试管中,加入足量 溶液,充分振荡。若固体无明显变化,则假设 成立;若有暗红色固体生成,则反应的离子方程式为 。
步骤3:取步骤2所得暗红色固体于试管中,滴加过量 ,振荡后静置。若溶液基本无色,则假设 成立;若溶液呈 ,则假设3成立。
(3)问题讨论
若固体产物中FeO含量较少,用步骤3方法难以确定。请你设计实验方案证明假设3成立(写出实验的操作步骤、现象与结论):
Ⅲ.拓展与延伸
有资料介绍“在含Fe2+的溶液中,先滴加少量新制饱和氯水,然后滴加KSCN溶液,溶液呈红色;若再滴加过量氯水,却发现红色褪去”。假设溶液中的+3价铁还能被氯水氧化为更高价的FeO42-”,试写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2013届河北省承德市联校高一上学期期末联考化学试卷 题型:实验题
某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究(可供选用的实验仪器及试剂如下)。
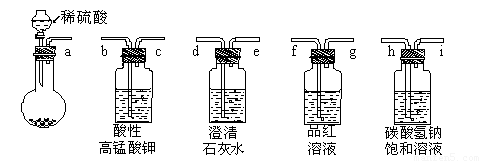
(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3: 。
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a— (每组选用仪器和试剂限用一次)。
(3)根据(2)的连接顺序进行实验,填写相应现象。
|
假设方案编号 |
相应现象 |
|
假设1 |
|
|
假设2 |
|
|
假设3 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究(可供选用的实验仪器及试剂如下)。

(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3: 。
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a— (每组选用仪器和试剂限用一次)。
(3)根据(2)的连接顺序进行实验,填写相应现象。
| 假设方案编号 | 相应现象 |
| 假设1 | |
| 假设2 | |
| 假设3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com