
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
| A、0.05mol/L | B、0.1mol/L | C、0.15mol/L | D、0.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
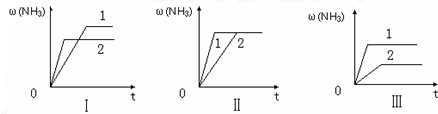
查看答案和解析>>
科目:高中化学 来源: 题型:
(08泉州五中模拟)设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.1molSiO2晶体内含有2NA个Si―O键
B.在0.1mol熔融KHSO4中,含有0.1NA个SO42-
C.在0.5L 1mol?L-1的盐酸中所含粒子总数为NA
D.46g四氧化二氮和二氧化氮的混合气体中含有原子数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com