
 价氧化物对应水化物酸性最强的酸是________________;
价氧化物对应水化物酸性最强的酸是________________; ____________。
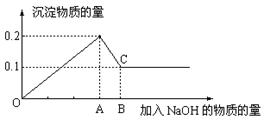
____________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
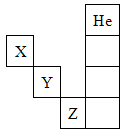
| A.①②③④ | B.①②③④⑤ | C.只有③⑤ | D.只有①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子最外层电子只有1个或2个的元素是金属元素 | |
B.16号元素原子的最 外层电子数是4号元素 外层电子数是4号元素 原子最外层电子数的四倍 原子最外层电子数的四倍 | C.11号元素与17号元素能形成XY2型化合物 |
| D.136C表示的碳原子核内有6个质子、7个中子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 结构和性质往往相似。化合物PH4I是一种白色晶体
结构和性质往往相似。化合物PH4I是一种白色晶体 ,下列对它的描述中正确的是
,下列对它的描述中正确的是| A.它是一种共价化合物 |
| B.在加热时此化合物不能分解为PH3和HI |
| C.这种化合物不能跟碱反应 |
D.该化合物可以由PH3和 HI化合而成 HI化合而成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a=b-1 | B.a=b-11 | C.b="a+25"  | D.b=a+30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.三种元素的简单阴离子的还原性按X、Y、Z的顺序增强 |
| B.单质的氧化性按X、Y、Z的顺序减弱 |
| C.原子半径按X、Y、Z的顺序减小 |
| D.气态氢化物的稳定性按X、Y、Z的顺序减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
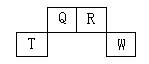
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| B.变价金属一定是过渡元素 |
| C.不含金属元素的化合物也可能是离子化合物 |
| D.显酸性的溶液中溶质只能是酸或强酸弱碱盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com