
科目:高中化学 来源: 题型:
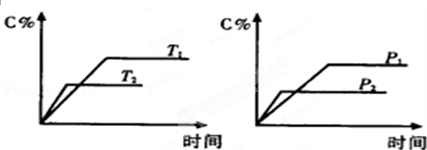
| A、a+b=c△H>0 |
| B、a+b>c△H<0 |
| C、a+b<c△H>0 |
| D、a+b<c△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积、浓度均为1 mol/L的硫酸和盐酸中,氢离子数之比为2:1 | ||
B、将wg质量分数为 a%的NaCl溶液蒸发掉
| ||
| C、将1体积c mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c mol/L | ||
| D、将5.85gNaCl晶体溶入1000mL水中,制得的NaCl溶液不为0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 1mol/L NaCl溶液 |
| B、75 mL 3mol/LKCl溶液 |
| C、150 mL 1mol/LK2SO4溶液 |
| D、75 mL 3mol/LFeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、37.3g |
| B、40.0g |
| C、45.0g |
| D、74.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据物质的元素组成,将纯净物分为单质和化合物 |
| B、通过镁、锌、铁分别与稀盐酸反应的实验现象,比较不同金属的活泼性强弱 |
| C、根据铁制品表面的锈可用稀盐酸溶解除去的事实,说明铁锈主要成分是酸性氧化物 |
| D、打开盛装浓盐酸的试剂瓶塞,观察现象,了解盐酸的某些物理性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Na+ | Al3+ | Cl- | X |
| 个数 | 3NA | 2NA | NA | m |
| A、NO3-、4NA |
| B、SO42-、4NA |
| C、OH-、4NA |
| D、SO42-、8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3g金属钠变为Na+时失去的电子数为NA |
| B、18gH2O所含的原子数目为NA |
| C、常温下22.4L氢气所含的原子数目为2NA |
| D、100℃、1.01×105Pa 32gO2所含的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com