
【题目】下列物质属于不等电子体的是( )
A.CH4和NH4+
B.B3H6N3和C6H6
C.CO2、N2O
D.H2O和CH4
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】为比较不同的催化剂对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.下列叙述中不正确的是( ) 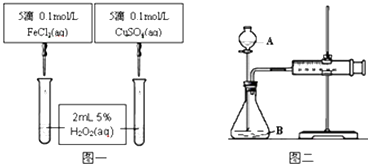
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置可测定反应产生的气体体积
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中所用仪器合理的是
A. 用 10 mL 量筒量取 5.2 mL 盐酸
B. 用 100 mL 量筒量取 5.2 mL 盐酸
C. 用托盘天平称取 25.02 g NaCl
D. 用 100 mL 容量瓶配制 50 mL 0.1 mol/L 的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种有机玻璃的结构简式为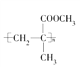 。下列关于它的叙述中不正确的是( )
。下列关于它的叙述中不正确的是( )
A. ![]() 在一定条件下发生缩聚反应即可合成该有机玻璃
在一定条件下发生缩聚反应即可合成该有机玻璃
B. 该有机玻璃能发生氧化反应
C. 合成该有机玻璃的原料可能有甲烷
D. 它在一定条件下发生水解反应时C—O键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池有广泛的应用,由方铅矿(PbS)制备铅蓄电池电极材料(PbO2)的方法如下:
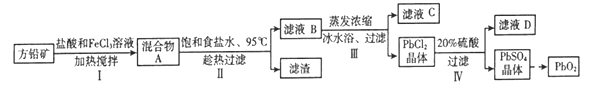
査阅资料:①PbCl2(s)+2Cl-(aq) ![]() PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
②Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9、7.0
③不同温度和浓度的食盐溶液中PbCl2的溶解度(g L-1):
| 20 | 40 | 60 | 100 | 180 | 260 | 300 |
13 | 3 | 1 | 0 | 0 | 3 | 9 | 13 |
50 | 8 | 4 | 3 | 5 | 10 | 21 | 35 |
100 | 17 | 11 | 12 | 15 | 30 | 65 | 95 |
(1)步骤I中FeCl3溶液与PbS反应生成PbCl2和S的化学方程式为__________________;
加入盐酸控制pH小于1.0的原因是________。
(2)步骤II中浸泡溶解时采用95℃和饱和食盐水的目的分别是____________、_____________。
(3)步骤III中将滤液B蒸发浓缩后再用冰水浴的原因是___________(请用平衡移动原理解释)。
(4)骤IV需用溶质质量分数为20%、密度为1.22 g·cm-3的硫酸溶液,现用溶质质量分数为98.3%、密度为1.84 g·cm-3的浓硫酸配制,需用到的玻璃仪器有___________ (填相应的字母)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒 F.胶头滴管
(5)用铅蓄电池为电源,采用电解法分开处理含有Cr2O72-及含有NO2-的酸性废水(最终Cr2O72-转化为Cr(OH)3, NO2-转化为无毒物质),其装置如下图所示。
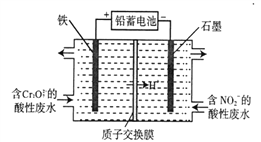
①左池中Cr2O72-转化为Cr3+的离子方程式是__________________。
②当阴极区消耗2 mol NO2-时,右池减少的H+的物质的量为______________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工原料。
Ⅰ、某学习小组同学设计了下图所示的实验装置(部分夹持仪器未画出),进行氨气实验室制备且探究氨气的还原性及产物的检验。
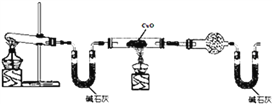
实验现象为:黑色CuO变为红色;干燥管中无水CuSO4粉末变为蓝色;同时生成一种无色无味无污染的气体。
(1)请写出大试管中反应的化学方程式_______________________________________。
(2)请写出氨气与CuO反应的化学方程式_________________________________________。
(3)该装置存在明显缺陷,请指出存在的问题______________________。
Ⅱ、哈伯因为将氮气和氢气在一定条件下合成氨气的成果面获得1918年诺贝尔化学奖。现将1molN2和3molH2充入一恒容的密闭容器中,使其在一定条件下达到平衡N2+3H2![]() 2NH3,下列哪些状态一定是达到平衡的状态?(_____)
2NH3,下列哪些状态一定是达到平衡的状态?(_____)
A.混合气体的平均相对分子质量不随时间改变而改变的状态
B.N2、H2、NH3的总物质的量不随时间改变而改变的状态
C.混合气体的密度不随时间改变而改变的状态
D.单位时间内0.1molNH3分解的同时,有0.05molN2生成的状态
Ⅲ、下图是一种电化学制备NH3的装置,图中陶瓷在高温时可以传输H+。
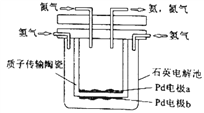
(1)H+经质子传输陶瓷由_____________流向_______________。(选填“a”或“b”)
(2)阴极发生的电极反应为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,都是由极性键构成的极性分子的是( )
A.NH3 和 H2OB.CO2 和 HClC.CH4 和 H2SD.HCN 和 BF3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com