
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
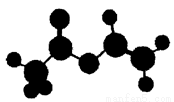
A. 该化合物的名称为乙酸乙酯
B. 该化合物与Br2的四氯化碳溶液不反应
C. 该化合物既能发生水解反应,又能发生氧化反应
D. 该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种
科目:高中化学 来源:2016-2017学年福建省三明市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于丙烯(CH3﹣CH=CH2)的说法正确的
A. 丙烯分子有7个σ键,1个π键
B. 丙烯分子中3个碳原子都是sp2杂化
C. 丙烯分子中最多有7个原子共平面
D. 丙烯分子中3个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源:2017届河北省张家口市高三第一学期期末教学质量监测化学试卷(解析版) 题型:简答题
铁和铜都是生产、生活中应用广泛的金属,能形成很多种合金和化合物。请回答:
(1)基态Cu+的价层电子排布图为________。基态Fe3+中有________种运动状态不同的电子。
(2)铁单质能形成Fe(CO)5,其熔点为-21℃,沸点为102.8℃。则Fe(CO)5晶体的类型为________,其σ键和π键的数目之比为________。与CO互为等电子体的离子符号为________(任写一种)。
(3)铜元素的焰色反应呈绿色,很多金属元素能发生焰色反应的微观原因为________。
(4)[Cu(NH3)4]SO4中,所含基态非金属原子的第一电离能由小到大的顺序为________。阴离子的空间构型为________,其中心原子的杂化轨道类型为________。
(5)铁单质的一种晶体的堆积模型为体心立方堆积,晶胞参数为apm;铜单质的一种晶体的堆积模型为面心立方最密堆积,晶胞参数为bpm。则两种晶体中,铁原子和铜原子的配位数之比为________,晶体的密度之比为________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2017届河北省张家口市高三第一学期期末教学质量监测化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法不正确的是
A. 4.0g氦气中含有的最外层电子数为4NA
B. 3.9g2H37Cl中含有的中子数为2.1NA
C. 标准状况下,11.2L丙烷中含有的非极性键数目为NA
D. 100mL1mol·L-1CH3COOH溶液中含有的分子数目大于0.1NA
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期第二次质检考试理科综合化学试卷(解析版) 题型:实验题
亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
I.NO+NO2+Ca(OH)2=Ca(NO2)2+H2O。
Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3-,MnO4-被还原为Mn2+。
Ⅲ.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32-能将I2还原为I-。
【制备氮氧化物】
(1)甲组同学拟利用如下左图所示装置制备氮氧化物。

①仪器X、Y的名称分别是______________、______________。
②装置B中逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为_____________________ ,若其他条件不变,增大硝酸的浓度,则会使逸出的气体中n(NO2)__________n(NO)(填“>”或“<”)。
【制备Ca(NO2)2】
⑵乙组同学拟利用装置B中产生的氮氧化物制备Ca(NO2)2,装置如上右图。
①装置C中导管末端接一玻璃球的作用是________________。
②装置D的作用是______________;装置E的作用是________________。
【测定Ca(NO2)2的纯度】
⑶丙组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
a.稀硫酸 b. c1mol·L-1的KI溶液 c.淀粉溶液
d.c2mol·L-1的Na2S2O3溶液 e.c3mol·L-1 的酸性 KMnO4 溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是______________(填字母)。
②利用Ca(NO2)2的氧化性来测定其纯度的步骤:准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,__________________(请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市、洪都中学、麻丘中学、十七中、桑海中学高二3月联考化学试卷(解析版) 题型:简答题
某同学设计如图所示的实验装置来粗略测定电石中碳化钙的质量分数。

(1)烧瓶中发生反应的化学方程式是_____________________。装置B和C的作用是______________________。烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了_______________________。容器A中弯曲的玻璃管的作用是__________________________。
(2)所用的电石质量不能太大,否则____________________;也不能太小,否则____________________。若容器B的容积为250mL,则所用的电石质量应在__________g左右(从以下数据选填:0.30、0.60、1.00、1.50、2.00)(气体体积以标准状况计)。
(3)实验室能否用启普发生器制乙炔,其原因是_______________________________。
(4)为了得到比较平稳的乙炔气流,常可用_____________代替水。
(5)实验中测得排入量筒中水的体积为VmL(以标准状况计),电石质量为mg。则电石中碳化钙的质量分数是_________________(不计算导管中残留的水;气体中饱和水蒸气也忽略不计)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市、洪都中学、麻丘中学、十七中、桑海中学高二3月联考化学试卷(解析版) 题型:选择题
实验中,所选取的分离装置与对应原理都正确的是 ( )

选项 | 目 的 | 装置 | 原 理 |
A | 氢氧化铁胶体的纯化 | ① | 胶体粒子不能通过滤纸,离子及小分子可以通过滤纸 |
B | 分离苯中的溴苯 | ③ | 苯(0.88 g/mL)和溴苯(1.5 g/mL)的密度不同 |
C | 粗盐提纯 | ①② | NaCl在水中的溶解度很大 |
D | 除去环己醇中的环烯 | ④ | 环己醇的沸点(161 ℃)与环己烯的沸点(83 ℃)相差较大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:填空题
下表是元素周期表中的一部分,根据A~M在周期表中的位置,回答下列问题:
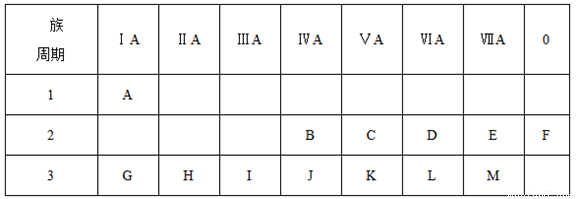
(1)表中元素,化学性质最不活泼的是_______,氧化性最强的单质是________,还原性最强的单质是____。(写元素符号或化学式)
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为________,酸性最强的化合物的化学式为___________,呈两性的化合物的化学式为___________。
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是_______(写化学式)。
(4)写出D、G、L对应的离子半径由大到小的顺序________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三一模理科综合化学试卷(解析版) 题型:简答题
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
已知:NaClO2饱和溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。Ba(ClO)2可溶于水。
利用如图所示装置进行实验。

(1)仪器a的名称为____,装置①的作用是____,装置③的作用是______。
(2)装置②中产生ClO2,涉及反应的化学方程式为________________;装置④中反应生成NaClO2的化学方程式为_______________。
(3)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③______;④低于60 ℃干燥,得到成品。如果撤去④中的冷水浴,可能导致产品中混有的杂质是________。
(4)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作与现象是:取少量晶体溶于蒸馏水,_____________________。
(5)为了测定NaClO2粗品的纯度,取上述粗产品10.0 g溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00 mL,试计算NaClO2粗品的纯度_____。(提示:2Na2S2O3+I2 Na2S4O6+2NaI)
Na2S4O6+2NaI)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com