
����(1)�뽫ʵ�������еı��(A��B����)�����Ӧ��ʵ�鷽���У�
|
ʵ�鷽�� |
ʵ�������� |
|
1����ɰֽ������þ�����ˮ��Ӧ������ӦҺ�еμӷ�̪ |
|
|
2�������Ƶ�H2S������Һ�еμ����Ƶ���ˮ |
|
|
3��������з�̪��Һ����ˮ��Ӧ |
|
|
4��þ����2 mol��L-1�����ᷴӦ |
|
|
5��������2 mol��L-1�����ᷴӦ |
|
|
6����AlCl3��Һ�еμ�NaOH��Һ������ |
|
|
ʵ�������¼ |
|
A������ˮ�棬�۳�һ��С����ˮ���������ƶ�����֮��ʧ����Һ���ɫ |
|
B��������������(���ڿ�����ȼ��)����Һ���dz��ɫ |
|
C����Ӧ��ʮ��ǿ�ң���������������ڿ�����ȼ�� |
|
D�����ҷ�Ӧ����������������ڿ�����ȼ�� |
|
E.���ɰ�ɫ��״�������̶�������ʧ |
|
F.���ɵ���ɫ���� |
����(2)�����Ϸ����У�δ�г�14�š�15����Ԫ�����ʵıȽϣ������������һ��ʵ�鷽�����ԱȽ�֮��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| NH3?H2O��Kb | Zn 2+��ȫ������pH | Zn��OH��2���ڼ��pH |
| 1.8��10-5 | 8.9 | ��11 |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���Ϻ���������������ѧ����ĩ������⻯ѧ�Ծ� ���ͣ�ʵ����
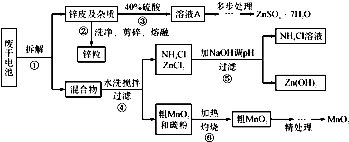
Ϊ̽��ͭ��Ũ����ķ�Ӧ��ij��ȤС�����������ʵ�顣
��ʵ��1��ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��
(1)��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ��
(2)��Ϩ��ƾ��ƺ���Ϊ�е��ܴ��ڣ�B�е�Һ�岻�ᵹ������ԭ���ǣ� ��
���װ��ǰ����������Ϊ��ʹװ���еIJ���������ȫ�����գ�Ӧ����ȡ�IJ����ǣ� ��
��ʵ��2��ʵ���з����Թ��ڳ��˲�����ɫ�����⣬��ͭ˿���滹�к�ɫ��������ɣ����п��ܺ�������ͭ��������ͭ����ͭ������ͭ��
�������ϣ�
��������ͭ�����Ի����»ᷢ������������ԭ��Ӧ����Cu2+��ͭ���ʣ��ڿ����г�����գ�����ת��Ϊ����ͭ��
����ͭ������ͭ�����¶�������ϡ���ᣬ�ڿ����г�����գ���ת��Ϊ����ͭ�Ͷ�������
Ϊ���о��ijɷ֣���С��ͬѧ���ռ����㹻���Ĺ������������ʵ�飺
(3)��������м��������Ƿ�ϴ�Ӹɾ���ʵ�鷽���ǣ� ��
(4)���������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У�
��
(5)��ȷ�����Ƿ�������ȫ�IJ����ǣ� ��
(6)�����չ�����һ�������Ļ�ѧ��Ӧ����ʽΪ�� ��
������泥�NH4ClO4���Ǹ��ϻ���ƽ�������Ҫ�ɷ֣�ʵ���ҿ�ͨ�����з�Ӧ��ȡ��
��������NaClO4(aq)+NH4Cl(aq) NH4ClO4(aq)+NaCl(aq)
NH4ClO4(aq)+NaCl(aq)
(7)���ð�����Ũ�������NH4Cl��������Ӧ����Ҫ��繩�Ⱦ��ܽ��У���ԭ����:
��
(8)����Ӧ�õ��Ļ����Һ��NH4ClO4��NaCl�����������ֱ�Ϊ0.30��0.l5��������ʵ��ܽ����������ͼ�����ӻ����Һ�л�ý϶�NH4ClO4�����ʵ���������Ϊ����������ƣ�����Ũ���� �����ˣ� �����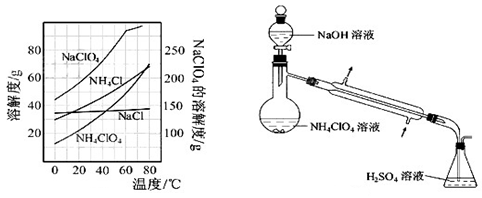
Ϊ�˲ⶨ��Ʒ��NH4ClO4�ĺ�����װ������ͼ��ʾ������װ�á������̶�װ������ȥ����ʵ�鲽�����£�
(9)������3�У�ȷȡ��24.00 mL H2SO4(aq)�IJ��������� ��
(10)��ʵ����ȷ�����ɵİ���ϡ������ȫ���յ�ʵ�鲽���� ����д�����ţ���
(11)�������ظ�ʵ��2~3�Σ���ԭ���� ��
(12)�����0.320 g�����к�NH4ClO4��ȷֵΪ0.095g����ʵ��ⶨ�����0.092g����ʵ��
��������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�������ʡ�����е���ʮ����ѧ������ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
��15�֣�ij��ѧ�о�С��Ϊ�ⶨNa2O2��Ʒ������Na2O���ʣ��Ĵ��ȣ����������ʵ�鷽������̽����
[ʵ��һ]ȡ��Ʒ0.100 g������ͼ��ʾʵ��װ�ý��вⶨ�����г�װ��ʡ�ԣ�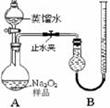
��1�����װ��A�����Եķ����� ����������������������������
��2������ʵ������й���������11.20 mL��������ɱ�״����������Ʒ��Na2O2�Ĵ���Ϊ������ ������������������������
[ʵ���]��Ʒ����ˮ��������ζ�
��3��ȡһ������Ʒ����ˮ��ϡ����250 mL������ʱ�����õ��IJ������������ձ��Ͳ������⣬�����õ�������������������������
��4��ȡ����������Һ��25.00 mL����һ��Ũ�ȵı�����ζ���ƽ��ʵ���¼���±���
| ʵ����� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| �����������mL�� | 23.00 | 24.98 | 25.00 | 25.02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�������ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��15�֣�ij��ѧ�о�С��Ϊ�ⶨNa2O2��Ʒ������Na2O���ʣ��Ĵ��ȣ����������ʵ�鷽������̽����
[ʵ��һ]ȡ��Ʒ0.100 g������ͼ��ʾʵ��װ�ý��вⶨ�����г�װ��ʡ�ԣ�
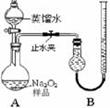
��1�����װ��A�����Եķ����� ����������������������������
��2������ʵ������й���������11.20 mL��������ɱ�״����������Ʒ��Na2O2�Ĵ���Ϊ������ ������������������������
[ʵ���]��Ʒ����ˮ��������ζ�
��3��ȡһ������Ʒ����ˮ��ϡ����250 mL������ʱ�����õ��IJ������������ձ��Ͳ������⣬�����õ�������������������������
��4��ȡ����������Һ��25.00 mL����һ��Ũ�ȵı�����ζ���ƽ��ʵ���¼���±���
|
ʵ����� |
��һ�� |
�ڶ��� |
������ |
���Ĵ� |
|
�����������mL�� |
23.00 |
24.98 |
25.00 |
25.02 |
�ɱ������ݿ�֪�������������ƽ��ֵΪ������������ ������mL�����ζ�ǰ������������Һ��ϴ��ƿ���Բⶨ�������������Ӱ���������������������� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
[ʵ�����]ʵ�����Աȷ���
��5��С��ͬѧ�Ա�����ʵ�鷢�֣�ʵ��һ��õ�Na2O2��Ʒ�Ĵ��ȱ�����ֵ����ƫС������������С��ͬѧ��Ϊ������ƫ����ɲ���ʧ���װ��ȱ������ģ������Ƿ�Ӧԭ���ϵ�ԭ�������Ϸ��֣�
Na2O2��ˮ��Ӧ������H2O2δ��ȫ�ֽ⡣
��д��Na2O2��ˮ����H2O2�Ļ�ѧ����ʽ����������������������������������������
������ʵ��һ�ԼӸĽ�������ʹ�ⶨ����ӽ�����ֵ��д���Ľ�������������������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com