
 在恒温条件下,将气体X、Y充入2L密闭容器中反应生成气体Z.若各气体的物质的量随时间变化曲线如图所示,下列描述正确的是( )
在恒温条件下,将气体X、Y充入2L密闭容器中反应生成气体Z.若各气体的物质的量随时间变化曲线如图所示,下列描述正确的是( )| A、前10s内 v(X)=0.08mol?L-1?s-1 | B、该反应的平衡常数K=32 | C、平衡时X、Y的转化率相同 | D、达到平衡后,将容器体积扩大为4L,平衡向逆反应方向移动 |
| c2(Z) |
| c(X)c(Y) |
| ||
| t |
| ||
| 10s |
| c2(Z) |
| c(X)c(Y) |
(
| ||||
|
| 1.20-0.40 |
| 1.20 |
| 1.00-0.20 |
| 1.00 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 2NH3,在一定条件下已达到平衡状态.
2NH3,在一定条件下已达到平衡状态. 2NH3(g)△H=-92.4KJ/mol
2NH3(g)△H=-92.4KJ/mol 2NH3(g)△H=-92.4KJ/mol
2NH3(g)△H=-92.4KJ/mol| 2-a |
| 2 |
| 2-a |
| 2 |
| 6-3a |
| 2 |
| 6-3a |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |
| ||
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省湛江市高三上学期普通高考测试(一)理综化学试卷(解析版) 题型:计算题
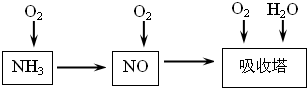
工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
|


 (1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(2)硝酸厂尾气常用的处理方法是催化还原法:催化剂存在时用H2将NO2还原为N2 。已知:
2H2(g)+O2(g)=2H2O(g) △H= a kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H= b kJ·mol-1
H2O(1)=H2O(g) △H= c kJ·mol-1
则反应2NO2(g)+4H2(g)=N2(g)+4H2O(1)的△H=_________。(用a、b、c表示)
(3)①合成氨反应的化学方程式为N2+3H2 2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的相对分子质量保持不变
E.1mol N≡N键断裂,同时1mol H—H键断裂
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L的密闭容器中,5min反应达平衡,n(N2)=1mol,n(H2)=1mol,n(NH3)=2mol,则反应速率v(N2)=________________,H2的平衡转化率=_________________;若保持容器的温度不变,在10min时将容器的容积压缩为lL,请在答题卡坐标图中,画出从反应开始至15min时c(NH3)随时间变化曲线示意图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com