
| A、11.2 g |
| B、2.8 g |
| C、5.6 g |
| D、无法计算 |


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
| A、氧化物:CO2、NO、SO2、H2O |
| B、碱:NaOH、KOH、Ba(OH)2、NH3?H2O、Na2CO3 |
| C、铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、碱性氧化物:Na2O、CaO、Mn2O7、Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
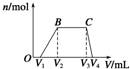 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH
| ||||
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4,则V A族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| B、第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3,则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| C、存在离子键的化合物是离子化合物,则存在共价键的是共价化合物 |
| D、KNO3溶于水时溶液温度无明显变化,则NH4NO3溶于水时溶液温度也无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6 |
| B、C3H10O |
| C、C4H8O2 |
| D、C5H10O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、SO42-一定存在 |
| B、该溶液中含CO32-离子的浓度为1 mol/L |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Cu2+、Ca2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、电池放电时,PbO2是负极;充电时,PbO2是电池的阳极 |
| B、负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C、放电时,PbO2得电子,被氧化 |
| D、电池放电时,溶液酸性增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com