
����Ŀ����ҵ�������е�һ����Ҫ��Ӧ��SO2��400��500��C�µĴ�����2SO2+O2![]() 2SO3������һ������Ӧ���ȵĿ��淴Ӧ��������ܱ�������ͨ��2molSO2���㹻����������������������з�Ӧ�������й�˵���д������
2SO3������һ������Ӧ���ȵĿ��淴Ӧ��������ܱ�������ͨ��2molSO2���㹻����������������������з�Ӧ�������й�˵���д������
A.ͨ�����Է�Ӧ������������߸÷�Ӧ�Ľ��г̶�
B.ʹ�ô�����Ŀ���Ǽӿ췴Ӧ���ʣ��������Ч��
C.�ﵽƽ��ʱ��SO2��SO3���������
D.��߷�Ӧ�¶ȣ�����ʵ��SO2����ȫת��
���𰸡�D
��������
A��ͨ���ı�Ӱ��ƽ���������������ѹǿ���£����ɴٽ�ƽ�������ƶ�����߸÷�Ӧ���еij̶ȣ���A��ȷ��
B��ʹ�ô����ӿ��˷�Ӧ���ʣ�������̴ﵽƽ�������ʱ�䣬��߷�ӦЧ�ʣ�ƽ�ⲻ���ƶ�����B��ȷ��
C���ﵽƽ��ʱ�����淴Ӧ������ȣ���SO2��SO3��������ȣ���C��ȷ��
D����Ϊ�ÿ��淴ӦΪ���ȷ�Ӧ����߷�Ӧ�¶ȣ�ƽ�������ƶ���SO2ת���ʽ��ͣ���������ȫת������D����
��ΪD��


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ĽṹΪ��ͼ��ʾ�������л��ﲻ���ܾ��е������ǣ� ��
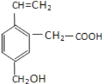
������̼ԭ�ӿ��ܹ��棻
����ʹ����KMnO4 ��Һ����ˮ��ɫ����ԭ����ͬ��
��1mol ���л���ֱ������� Na ��NaHCO3 ��Ӧ�����������ڱ�����������ȣ�
���ܷ���������Ӧ��
���ܷ����Ӿ۷�Ӧ��
��1mol ���л�����ȫȼ������ CO2 ��H2O ���� O2 �����Ϊ 280L����״����
A.�٢�B.�ڢ�C.�ۢ�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ����
A.��0.1mol![]() CH3COOH��Һ�м�������ˮ����Һ��
CH3COOH��Һ�м�������ˮ����Һ��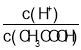 ��С
��С
B.��CH3COONa��Һ��20��������30�棬��Һ��![]() ����
����
C.�������м��백ˮ�����ԣ���Һ��![]() >1
>1
D.��0.1mol/L��NaOH���¶������80�棬��Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ��ֵ�һ����Ȼ��ʮ������������Al��Ca��Cu��Fe���ֽ���Ԫ����ɡ���ش��������⣺
(1)��̬��ԭ�Ӽ۵����Ų�ʽΪ_________���ӽṹ�Ƕ�������Fe2+�ױ�������Fe3+��ԭ����________________��
(2)SCN�����ӿ����� Fe3+�ļ��飬���Ӧ���������֣��ֱ�Ϊ������(H-S-C��N)����������(H-N=C=S)��
��д���� SCN����Ϊ�ȵ������һ����_____(���ӻ�����)��
���������������ԭ�ӵ��ӻ���ʽΪ_____��
����������ķе��������е�ߵ�ԭ����____________________________��
(3)���Ƶ�Cu(OH)2�����ڹ����İ�ˮ�����ɵ������[Cu(NH3)4](OH)2�к��еĻ�ѧ�������� _____________________��1 mol�������к��� ____________________��������
(4)CaF2����ľ�����ͼ��ʾ����֪��CaF2������ܶ�Ϊ�� g��cm��3��NA���������ӵ�������ֵ��CaF2������Ca2����F��֮�������˼��(d)Ϊ ______________pm(�г�����ʽ����)��
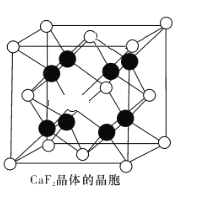
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�÷���ʵ��Ŀ���ǣ� ��
Ŀ�� | ��ͭ�ľ��� | ��֤NaCl��Һ������̪���IJ��� | ������Ʒ�϶�ͭ | ����ԭ��� |
װ�� |
|
|
|
|
ѡ�� | A | B | C | D |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CCTV��������30�����н��ܣ����߹���������ҹ����ֳ���謹ɻ�����ȫ������蝹��ȶ�������ReS2���ȶ�����������Re2O7����ҵ�ϣ�����ұ��ͭ�ķ�Һ����ȡ画���������������£����ָ�����ʡ�ԣ���ڷ�Һ����ReO4-��ʽ���ڣ���
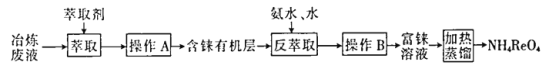
�ش��������⣺
��1��NH4ReO4�������泥����Ԫ�ػ��ϼ�Ϊ_________________��
��2������A��������_____________��
����ȡ������ȡ��Ӧ���е����ʣ�______������ţ���
����ȡ��������ˮ ����ȡ�����ܶȴ���ˮ
��ReO4-����ȡ���е��ܽ�ȴ�����ˮ�е��ܽ�� ����ȡ������ReO4-������Ӧ
��3����������ȡ���У����백ˮ��ˮ��Ŀ����_________________��
��4���ڸ����¸����立ֽ�����Re2O7����������ԭRe2O7���Ʊ��ߴ���覆ۡ�
��д�������立ֽ�����Re2O7�Ļ�ѧ����ʽ_____________________��
�ڹ�ҵ�ϣ�����������ԭRe2O7�Ʊ�画���������蝹���������������ʵ������H2���������ۼ���������ԭ����_____________________��
��5����ҵ�ϣ��������պ�ReS2�Ŀ�ۣ������Ʊ�R2O7���Ժ�ReS2�Ŀ�ʯԭ������48.4tRe2O7��������ת��__________mol���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�п��ܴ��ڵ���ƽ�⡢ˮ��ƽ��ͳ����ܽ�ƽ�⡣������ѧ֪ʶ�ش��������⣺
��1�����з����У�����ʹ0.10mol/LCH3COOH��Һ��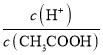 ֵ����Ĵ�ʩ��_______________������ţ���
ֵ����Ĵ�ʩ��_______________������ţ���
a.��ˮϡ��b.��������CH3COONa���� c.��������������d.ͨ������HCl���� e.�������ռ���Һ f.�����¶�
��2��t��ʱ��ˮ�����ӻ�����Kw=1��10-12��
�ٸ��¶��£���100���pH=a��H2SO4��Һ��1���pH=b��NaOH��Һ��Ϻ���Һ�����ԣ���a+b=_________��
�ڸ��¶��£�pH=2��ij��HA��Һ��pH=10��NaOH��Һ�������Ϻ����Һ��pH=5���Է�����ԭ��_______________________���û����Һ�У�c(A-)��c(Na+)=______________________mol/L������ֵ����
��3��25���£���Ũ�Ⱦ�Ϊ0.1mol/L��������Һ��a��NaHCO3��b��NaClO��c��CH3COONa������֪25��ʱ���볣����H2CO3 K1=4.4��10-7��K2=4.7��10-11��HClO K=3.0��10-8��CH3COOH K=1.8��10-5��
��������ҺpH��С�����˳��Ϊ��_______________________________������ţ���
����Һa��pH����8������Һ��c(H2CO3)_____c(CO32-)�����������������=������
��4����֪25��ʱ��Ksp(AgCl)=1.8��10-10���ֽ������Ȼ����ֱ���룺
a��100mL����ˮ�У�
b��100mL0.2mol/LAgNO3��Һ�У�
c��100mL0.1mol/L�Ȼ�����Һ�У�
d��100mL0.1mol/L������Һ�С�
��ֽ�������ͬ�¶���������Ũ���ɴ�С��˳����________________����д��ţ���b�������ӵ�Ũ��Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����[aX��bY]Ϊa��X����b��Y����ɵ�һ���������壬NAΪ�����ӵ�������ֵ������˵������ȷ����
A.H2(g)��![]() O2(g)=H2O(l)����H����286 kJ��mol1����ÿ1 mol [H2(g)��
O2(g)=H2O(l)����H����286 kJ��mol1����ÿ1 mol [H2(g)��![]() O2(g)]����1 mol [H2O(l)]����286 kJ
O2(g)]����1 mol [H2O(l)]����286 kJ
B.Cr2O72-��ne��14H+=2Cr3+��7H2O����ÿ����1 mol Cr3+ת�Ƶ�����Ϊ3NA
C.Al3+��4OH=[Al(OH)4]��˵��1 mol Al(OH)3�����H+��ΪNA
D.1 mol CO2��NaOH��Һ��ȫ��Ӧ����n(CO32-)��n(HCO3-)��n(H2CO3)��1 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���![]() ��Һ�ֱ�ζ�
��Һ�ֱ�ζ�![]() ������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����
������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����![]()
![]()
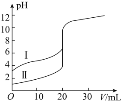
A.���ʾ���ǵζ����������
B.![]() ʱ���ζ��������ĵ�
ʱ���ζ��������ĵ�![]() С��
��![]()
C.![]() ʱ��������Һ��
ʱ��������Һ��![]()
D.![]() ʱ��������Һ��
ʱ��������Һ��![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com