


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
| A、H2SO4=2H++SO42- |
| B、Al2(SO4)3=2Al3++3 SO42- |
| C、NaHCO3=Na++H++CO32- |
| D、Ba(OH)2=Ba2++2 OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的压强不变 |
| B、混合气体的密度不变 |
| C、每消耗2molB,同时消耗1molC |
| D、C和D的浓度比不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
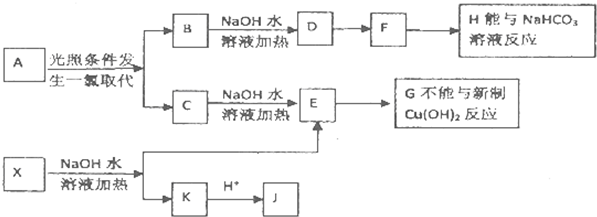
查看答案和解析>>
科目:高中化学 来源: 题型:
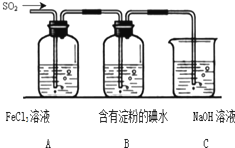 为探究SO2气体的还原性某兴趣小组设计了如图装置图:
为探究SO2气体的还原性某兴趣小组设计了如图装置图:查看答案和解析>>
科目:高中化学 来源: 题型:
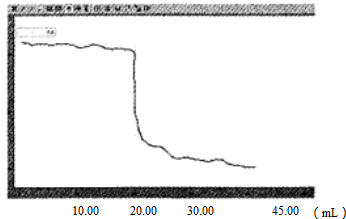
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol/L H2SO4 溶液 |
| B、2mol/L NaOH溶液 |
| C、2mol/L MgSO4溶液 |
| D、硅酸溶胶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com