
 (2010?德阳模拟)某有机物A的结构简式如右图所示,下列有关叙述正确的是( )
(2010?德阳模拟)某有机物A的结构简式如右图所示,下列有关叙述正确的是( )

科目:高中化学 来源: 题型:
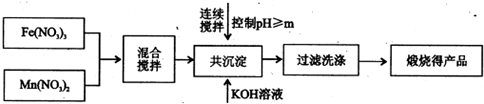
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
| ||
| x |
| 2 |
| 1 |
| 2 |
| a+b |
| x |
| 1 |
| 2 |
| a+b |
| x |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com