
【题目】异戊二烯(2—甲基—1,3—丁二烯)是一种重要的有机化工原料。
(1)其结构简式为______________,官能团的名称是__________________。推测它在空气中燃烧时的现象___________________________________________________。
(2)下列是关于其性质的描述。在你认为肯定错误的地方划出横线(不能确定就不划出)。如“熔点___℃”。通常状态下是无色刺激性液体,沸点34℃。能溶于水,易溶于乙醇和乙醚。在贮藏过程中易发生氧化和聚合。又已知,化合物X与异戊二烯具有相同的分子式,是一种没有支链的炔烃,X可能的结构简式为_________________________________________________。
【答案】 ![]() 碳碳双键 剧烈燃烧,有明亮的火焰,产生浓烟 能溶于水 CH≡CCH2CH2CH3、CH3C≡CCH2CH3
碳碳双键 剧烈燃烧,有明亮的火焰,产生浓烟 能溶于水 CH≡CCH2CH2CH3、CH3C≡CCH2CH3
【解析】试题分析:(1)根据异戊二烯的系统命名写结构简式;烯烃的官能团是碳碳双键;根据异戊二烯含碳量高于烷烃分析燃烧的现象;(2)烃均难溶于水;异戊二烯的不饱和度是2,X是炔烃,所以只含有1个碳碳叄键;
解析:(1)异戊二烯的系统命名是2—甲基—1,3—丁二烯,所以结构简式是![]() ;异戊二烯的官能团是碳碳双键;烯烃中碳的质量分数较大,异戊二烯在空气中燃烧时的现象是剧烈燃烧,有明亮的火焰,产生浓烟;(2)碳原子数大于4,所以常温下是液体,烃均难溶于水,易溶于有机溶剂,含有碳碳双键,所以易发生氧化反应和聚合反应,所以错误的是能溶于水;异戊二烯的不饱和度是2,X是炔烃,只含有1个碳碳叄键,所以没有支链的可能结构简式是CH≡CCH2CH2CH3、CH3C≡CCH2CH3;
;异戊二烯的官能团是碳碳双键;烯烃中碳的质量分数较大,异戊二烯在空气中燃烧时的现象是剧烈燃烧,有明亮的火焰,产生浓烟;(2)碳原子数大于4,所以常温下是液体,烃均难溶于水,易溶于有机溶剂,含有碳碳双键,所以易发生氧化反应和聚合反应,所以错误的是能溶于水;异戊二烯的不饱和度是2,X是炔烃,只含有1个碳碳叄键,所以没有支链的可能结构简式是CH≡CCH2CH2CH3、CH3C≡CCH2CH3;


科目:高中化学 来源: 题型:
【题目】某一元醇A和一元羧酸B形成的酯的式量为212,分子内碳原子数是氢、氧原子数之和.该酯不能使溴的四氯化碳溶液褪色,又知A可氧化得B.则下列叙述中,正确的是( )
A.A的式量比B大14
B.B的式量比A大16
C.该酯中一定不含双键等不饱和键
D.酯,A,B三种物质的分子中都含一种相同的式量大于45的原子团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为A、B两种固体物质的溶解度随温度变化的曲线。请回答:
(1)30 ℃时,A、B两物质的溶解度________。
(2)20 ℃时,A物质的溶解度________B物质的溶解度(填“>”、“<”或“=”)。
(3)40 ℃时,将A、B各15 g分别加到均盛有50 g水的两只小烧杯中,充分搅拌后,________物质有剩余(填“A”或“B”)。

(4)现有50 ℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是________(填序号)。
①降低温度 ②升高温度 ③加入A物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.酸碱中和滴定终点的pH值一定等于7
B.滴定实验中锥形瓶不可用待测液润洗
C.滴定实验中,KMnO4溶液应放在碱式滴定管中
D. 用盐酸滴定NaOH溶液的滴定曲线如图所示
用盐酸滴定NaOH溶液的滴定曲线如图所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是( )
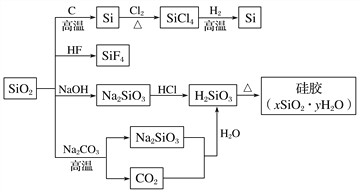
A. SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物
B. Na2SiO3俗称水玻璃
C. 硅胶可用作袋装食品、瓶装药品干燥剂和催化剂的载体
D. 天然单质硅广泛用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是___________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):______>_____;比较g、h的最高价氧化物对应水化物的酸性强弱:______>______。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。

回答下列问题:
(1)A与E形成的化合物的化学式是 。
(2)B的最高价氧化物化学式为 ,C的元素名称为 ,
D的单质与水反应的方程式为_ 。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是 ,有关反应的离子方程式为 ; 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com