

请回答下列问题:
(1)配平反应①的离子方程式(配平系数填入相应的方框内).
(2)用Na2S2O3标准液滴定I2时(反应④)选用的指示剂是________.
(3)取b0mL待测液,用H2SO4酸化,再用a1mol·L-1的标准KMnO4溶液滴定其中的H2O2,耗用KMnO4体积b1mL,(滴定过程中KMnO4不与![]() 反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
此时![]()
与H2O2都能与KI反应生成I2(反应②和③).再用a2mol·L-1Na2S2O3标准液滴定生成I2,耗用Na2S2O3为b2mL.
请根据上述实验数据计算过氧乙酸浓度(用含a1,a2,b0,b1,b2的代数式表示).c0=___________
(4)为计算待测液中![]() 浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
科目:高中化学 来源: 题型:


| a2b2-5a1b1 |
| 2b0 |
| a2b2-5a1b1 |
| 2b0 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:043
抗击:“非典”期间,过氧乙酸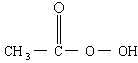 是广为使用的消毒剂.它可由
是广为使用的消毒剂.它可由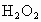 和冰醋酸反应制取,所以在过氧乙酸中常含有残留的
和冰醋酸反应制取,所以在过氧乙酸中常含有残留的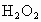 .测定产品中过氧乙酸浓度
.测定产品中过氧乙酸浓度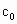 .涉及下列反应:
.涉及下列反应:
①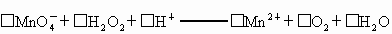
②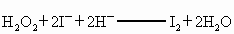
③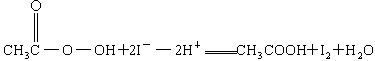
④
请回答以下问题:
(1)配平反应①的离子方程式(配乎化学计量数填入以下方框内):

(2)用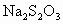 标准溶液滴定
标准溶液滴定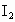 时(反应④)选用的指示剂是__________.
时(反应④)选用的指示剂是__________.
(3)取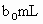 待测液,用硫酸使溶液酸化,再用浓度为
待测液,用硫酸使溶液酸化,再用浓度为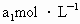 标准溶液滴定其中的
标准溶液滴定其中的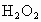 ,耗用的
,耗用的 体积为
体积为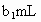 (反应①,滴定过程中
(反应①,滴定过程中 不与过氧乙酸反应).
不与过氧乙酸反应).
另取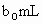 待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的
待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的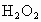 都能跟KI反应生成
都能跟KI反应生成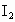 (反应②和③).再用浓度为
(反应②和③).再用浓度为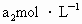 的
的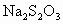 标准溶液滴定生成的
标准溶液滴定生成的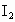 ,耗用
,耗用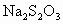 溶液体积为
溶液体积为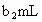 .
.
请根据上述实验数据计算过氧乙酸的浓度(用含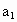 、
、 、
、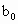 、
、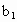 、
、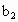 的代数式表示).
的代数式表示).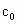 =__________.
=__________.
(4)为计算待测液中过氧乙酸的浓度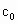 ,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).
,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).
查看答案和解析>>
科目:高中化学 来源: 题型:
①_____![]() +_____H2O2+______H+——_____Mn2++______O2+______H2O
+_____H2O2+______H+——_____Mn2++______O2+______H2O
②H2O2+2I-+2H+====I2+2H2O
③CH3COOOH+2I-+2H+====CH3COOH+I2+H2O
④I2+2![]() ====S4O62-+2I-
====S4O62-+2I-
请回答以下问题:
(1)配平反应①的离子方程式(配平化学计量数依次填在下面所给直线上):
![]() +_____H2O2+_____H+——______Mn2++_____O2+_____H2O
+_____H2O2+_____H+——______Mn2++_____O2+_____H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是________。
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol·L-1的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中,KMnO4不与过氧乙酸反应)。
另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(反应②和③)。再用浓度为a2 mol·L-1的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度。
c0=________(用含a1、a2、b0、b1、b2的代数式表示)。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果______(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源:2011届江西省安福中学高三年级入学考试 题型:单选题
抗击“非典”期间,过氧乙酸(CH3COOOH)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
①□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
②H2O2+2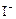 +2H+ =I2+2H2O
+2H+ =I2+2H2O
③CH3COOOH+2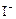 +2H+= CH3COOH+I2+H2O
+2H+= CH3COOH+I2+H2O
④I2+ 2S2O32- =2I-+ S4O62-
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填入以下方框内):
□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
(2)用单线桥法在下面已配平的化学方程式上标出电子转移的方向和数目:
□MnO4-+□H2O2+□H+ =□Mn2++□O2↑十□H2O
(3)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是____________________。
(4)取b0L待测液,用硫酸使溶液酸化,再用浓度为a1 mol·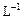 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2mol·
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2mol·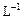 的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2L。请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。c0= _______________ mol·
的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2L。请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。c0= _______________ mol·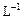 。
。
(5)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 ________(填是或否)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com