
【题目】小颖同学用如图所示装置研究原电池原理,下列说法错误的是( )
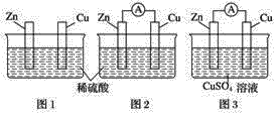
A.若将图1装置的Zn、Cu直接接触,Cu片上能看到气泡产生
B.图2装置中![]() 向Cu片移动
向Cu片移动
C.若将图2中的Zn片改为Mg片,Cu片上产生气泡的速率加快
D.图2与图3中正极生成物的质量比为1:32时,Zn片减轻的质量相等
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气的脱硝(除![]() )技术和脱硫(除
)技术和脱硫(除![]() )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
(1)工业上可以采用“质子膜电解槽”对烟气进行脱硫脱硝,其工艺如图甲所示:
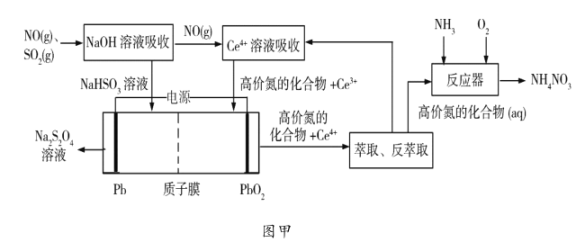
①![]() 溶液吸收
溶液吸收![]() 主要反应的化学方程式为___________;
主要反应的化学方程式为___________;
②电解的主要目的是______________,阴极的电极反应式为______________;
③“高价氮的化合物”中NO2在反应器中发生化合反应的化学方程式为______;
(2)利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的![]() 与活性焦炭反应生成
与活性焦炭反应生成![]() 和
和![]() ,当生成
,当生成![]() 时,转移电子的物质的量为__________
时,转移电子的物质的量为__________![]() ;
;
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入![]() 的
的![]() 乳浊液中,发生的反应如下:
乳浊液中,发生的反应如下:![]() ,
,![]() ,改变
,改变![]() ,
,![]() 的去除率变化情况如图乙所示。
的去除率变化情况如图乙所示。
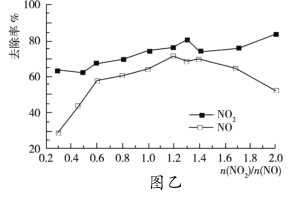
①当![]() 大于1.4时,
大于1.4时,![]() 去除率升高,但
去除率升高,但![]() 的去除率却降低。其可能的原因是__;
的去除率却降低。其可能的原因是__;
②![]() 和
和![]() 发生的主要反应为
发生的主要反应为![]() 。保持
。保持![]() 的初始浓度不变,改变
的初始浓度不变,改变![]() ,将反应后的混合气体通入
,将反应后的混合气体通入![]() 乳浊液中吸收。为节省
乳浊液中吸收。为节省![]() 的用量,又能保持
的用量,又能保持![]() 去除效果,则
去除效果,则![]() 合适的值约为___________;
合适的值约为___________;
(4)已知:![]() ,
,![]() ,则
,则![]() ______________________。
______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是
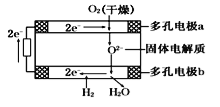
A. 有O2放电的a极为电池的负极
B. O2-移向电池的正极
C. b极对应的电极反应为2H2-4e-+2O2-=2H2O
D. a极对应的电极反应为O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是重要的能源物质,其制备、应用与转化是研究的热点。
(1) 利用合成气制备二甲醚主要包含三个反应:
CO(g)+2H2(g)=CH3OH(g);ΔH=-90.4 kJ·mol-1
2CH3OH(g)=CH3OCH3(g)+H2O(g);ΔH=-23.4 kJ·mol-1
CO(g) +H2O(g)=H2(g)+CO2(g);ΔH=-41.0 kJ·mol-1
则3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g);ΔH=________。
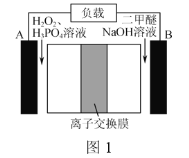
(2) 某二甲醚/双氧水燃料电池的工作原理如图1所示。电池工作时,电极A附近溶液pH________(填“减小”“增大”或“不变”);电极B的电极反应式为_____________。
(3) 二甲醚催化羰化制备乙醇主要涉及以下两个反应:
反应Ⅰ:CO(g)+CH3OCH3(g)=CH3COOCH3(g);ΔH1
反应Ⅱ:CH3COOCH3(g)+2H2(g)=CH3CH2OH(g)+CH3OH(g);ΔH2
反应Ⅰ、Ⅱ的平衡常数的对数lg K1、lg K2与温度的关系如图2所示;在固定CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图3所示。

① ΔH1________(填“>”“<”或“=”)0。
②300~400 K时,CH3CH2OH物质的量分数随温度升高而降低的原因是________。
③ 600~700 K时,CH3COOCH3物质的量分数随温度升高而降低的原因是________。
④ 400 K时,在催化剂作用下,反应一段时间后,测得CH3CH2OH物质的量分数为10%(图3中X点)。不改变原料比、温度和压强,一定能提高CH3CH2OH物质的量分数的措施有________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国北卡罗来纳大学的一项新研究表明,一种名为EIDD2801的新药有望改变医生治疗新冠肺炎的方式,有效减少肺损伤。其结构简式如图,下列有关EIDD2801的说法不正确的是( )

A.EIDD2801包含的含氧官能团有4种
B.EIDD2801分子中所有原子可能在同一平面上
C.EIDD2801一定条件下能和乙二酸发生聚合反应
D.EIDD2801能够使酸性高锰酸钾溶液或溴水等褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素,Y是地壳中含量最高的元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )
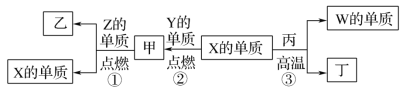
A.反应③为工业制粗硅的原理
B.Z位于元素周期表第三周期ⅡA族
C.4种元素的原子中,Y原子的半径相对最小
D.甲、丙、丁均为酸性氧化物,可以与碱反应得到对应盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素的原子半径的相对大小、最高正价或最低负价的变化如下图所示,下列分析正确的是( )

A.![]() 、
、![]() 的简单离子半径大小:
的简单离子半径大小:![]()
B.元素的金属性:![]()
C.元素的非金属性:![]()
D.![]() 、
、![]() 、
、![]() 和
和![]() 四种元素能形成离子化合物
四种元素能形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示实验,回答问题:
(1)实验①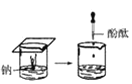 观察到的现象是________________________。实验②
观察到的现象是________________________。实验②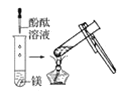 观察到的现象是________________________。
观察到的现象是________________________。
(2)实验③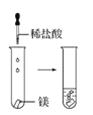 观察到的现象是________________________。实验④
观察到的现象是________________________。实验④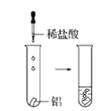 观察到的现象是________________________。
观察到的现象是________________________。
(3)由上述实验,你能得出的结论是________________________。
(4)请总结同周期元素金属性的变化规律__________,并用原子结构解释其原因_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com