
����Ŀ���������������Ļ��Գɷ֣����ڿ�ǻ�в������ոУ��ܹ���Ѫѹ�͵��̴��Ĺ�Ч�������ںܴ�̶���Ԥ�����ಡ��Ҳ�ܻ��⼡��ؽ���ʹ����������������ͨʽ���Ա�ʾΪ![]() (RΪ����)������һ���������������J�ĺϳ�·����ͼ��ʾ��
(RΪ����)������һ���������������J�ĺϳ�·����ͼ��ʾ��
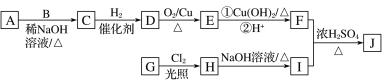
��֪����A��B��E��Ϊͬϵ�����A�ķ���ʽΪC5H10O��B����Է�������Ϊ44��A��B�ĺ˴Ź���������ʾ��������塣
��J�ķ���ʽΪC15H22O4��
��R1CHO��R2CH2CHO![]()
![]() ��
��
�ش��������⣺
(1)G�����������ŵ�����Ϊ__________��
(2)��A��B����C�Ļ�ѧ����ʽΪ__________��
(3)��C����D�ķ�Ӧ����Ϊ________��D�Ļ�ѧ����Ϊ_________��
(4)��H����I�Ļ�ѧ����ʽΪ________��
(5)��G��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵĹ���_____��(���������칹)�����к˴Ź���������ʾ��������_______(д�ṹ��ʽ)��
���𰸡��Ѽ���(��)�ǻ� (2)(CH3)3CCHO��CH3CHO![]()
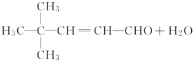 �ӳɷ�Ӧ(��ԭ��Ӧ) 4,4-����-1-�촼
�ӳɷ�Ӧ(��ԭ��Ӧ) 4,4-����-1-�촼 ![]() ��2NaOH
��2NaOH![]()
![]() ��NaCl��H2O 8
��NaCl��H2O 8 ![]()
��������
������J�ķ���ʽΪC15H22O4�����J�ĽṹΪ ����RΪ��C6H13����˽������ͼ֪��IΪ
����RΪ��C6H13����˽������ͼ֪��IΪ ��FΪC6H13COOH�����GΪ
��FΪC6H13COOH�����GΪ ��HΪ
��HΪ �������֪��Ϣ��B����Է�������Ϊ44��B�˴Ź���������ʾ������壬��BΪCH3CHO��A��BΪͬϵ���AΪC4H9CHO��A�ĺ˴Ź���������ʾ������壬��AΪ(CH3)3CCHO��CΪ(CH3)3CCH=CHCHO��DΪ(CH3)3CCH2CH2CH2OH��EΪ(CH3)3CCH2CH2CHO��FΪ(CH3)3CCH2CH2COOH���ݴ˷�������
�������֪��Ϣ��B����Է�������Ϊ44��B�˴Ź���������ʾ������壬��BΪCH3CHO��A��BΪͬϵ���AΪC4H9CHO��A�ĺ˴Ź���������ʾ������壬��AΪ(CH3)3CCHO��CΪ(CH3)3CCH=CHCHO��DΪ(CH3)3CCH2CH2CH2OH��EΪ(CH3)3CCH2CH2CHO��FΪ(CH3)3CCH2CH2COOH���ݴ˷�������
��1��GΪ �����������ŵ����Ѽ���(��)�ǻ����ʴ�Ϊ���Ѽ���(��)�ǻ���
�����������ŵ����Ѽ���(��)�ǻ����ʴ�Ϊ���Ѽ���(��)�ǻ���
��2��AΪ(CH3)3CCHO��BΪCH3CHO��A��B����C�Ļ�ѧ����ʽΪ(CH3)3CCHO��CH3CHO![]()
 ��
��
��3��CΪ(CH3)3CCH =CHCHO��DΪ(CH3)3CCH2CH2CH2OH��C�����������ӳɷ�Ӧ����D��DΪ(CH3)3CCH2CH2CH2OH������Ϊ4��4-����-1-�촼���ʴ�Ϊ���ӳ�(��ԭ)��4��4-����-1-�촼��
��4�� ������������Һ�з���ˮ�ⷴӦ����I����ѧ����ʽΪ
������������Һ�з���ˮ�ⷴӦ����I����ѧ����ʽΪ![]() ��2NaOH
��2NaOH![]()
![]() ��NaCl��H2O���ʴ�Ϊ��
��NaCl��H2O���ʴ�Ϊ��![]() ��2NaOH
��2NaOH![]()
![]() ��NaCl��H2O��
��NaCl��H2O��
��5��GΪ ��G��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵ���
��G��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵ���![]() ��
��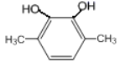 ��
�� ��
�� ��
��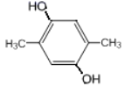 ��
��![]() ��
��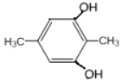 ��
�� ��8�֣����к˴Ź���������ʾ2������
��8�֣����к˴Ź���������ʾ2������![]() ���ʴ�Ϊ��8��
���ʴ�Ϊ��8��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��ʵ��ó��Ľ�����ȷ���ǣ� ��
A.�ò�˿պȡ����Һ���ڻ��������գ�����ʻ�ɫ����ԭ��Һ�к�Na+����K+
B.�����Һ�м��Ȼ�����Һ�����ɰ�ɫ�������ټ�ϡ���ᣬ�������ܽ⣬��ԭ��Һ�к���SO![]()
C.�����Һ�м�ϡ���ᣬ������ɫ��ζ���壬����Һ�к�CO![]()
D.�����Һ�м�NaOH��Һ���а�ɫ�������ɣ���������NaOH��Һ������ȫ���ܽ⣬��ԭ��Һ�п��ܺ�Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�����ȫȼ�գ�����CO2��H2O����12g���л������ȫȼ�ղ���ͨ��Ũ���ᣬŨ��������14.4g����ͨ����ʯ�ң���ʯ������26.4g������л���ķ���ʽΪ
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƽ�ֳ������Ƽ�����ҹ���ѧ����ר�Һ�°���1943�귢���ġ��˷�������ʳ�������ʸߡ��Ի�������Ⱦ�١������ɱ��͵��ŵ㡣���Ʊ����漰����������Ӧ��NaC1+H2O+CO2+NH3===NaHCO3��+NH4Cl��2NaHCO3![]() Na2CO3+CO2��+H2O��
Na2CO3+CO2��+H2O��
(1)��̬��ԭ�ӵĵ����Ų�ʽΪ______��C��N��O����Ԫ�ص�һ�������ɴ�С��˳��Ϊ____��
(2)��H2O��CO2��NH3���ַ���������V�η��ӵ���_______��
���ڳ��³�ѹ�£�1���ˮ���ܽ�700���NH3�����ܽ�0.8���CO2���Խ�����ԭ��_________��
(3)Cu(NH3)2Cl2������ͬ���칹�壬����һ�ֿ�����ˮ������ֻ�������________(���������������Ǽ�����)���ӣ��ɴ���֪[Cu(NH3)4]2+�Ŀռ乹����________��
(4)��Ҫȷ��Na2CO3�����Ǿ��廹�ǷǾ��壬��ɿ��ķ�����_____��
��������ʵ����֧��Na2CO3�ľ�������Ϊ���Ӿ������______(����ĸ)��
a���۵�Ϊ851�� b�������д���Na+��CO![]()
c��������ˮ d�������д������Ӽ������ۼ�
(5)�ơ�����Ԫ�ؿ��γ����ֳ������������һ�ֵľ�������ͼ��ʾ�����������Ļ�ѧʽΪ________������������Ϊd pm���������ܶ�Ϊ![]() �����ӵ�����NA=______(�ú�d�����Ĵ���ʽ��ʾ)��
�����ӵ�����NA=______(�ú�d�����Ĵ���ʽ��ʾ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Al��CuO��Fe2O3��ɵĻ����10.0 g����250 mLijŨ�ȵ������У��������ȫ�ܽ⣬���ټ���250 mL 2.0 mol��L-1��NaOH��Һʱ���õ��ij�����ࡣ�������Ũ��Ϊ(����)
A.0.5 mol��L-1B.3.0 mol��L-1C.2.0 mol��L-1D.1.0 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������(K2FeO4)��һ�ֱ�Cl2��O3��KMnO4�����Ը�ǿ�Ķ��ˮ����������ҵ�Ͽ����Ƶø�������[���ӷ�ӦΪFe(OH)3��ClO����OH����![]() ��Cl����H2O]��Ȼ���ڸ���������Һ�м���һ������KOH��������������ء�����˵������ȷ����( )
��Cl����H2O]��Ȼ���ڸ���������Һ�м���һ������KOH��������������ء�����˵������ȷ����( )
A.��������ܳ�ȥˮ���ܽ��H2S��
B.��ҵ���Ʊ���������ʱÿ����1mol��ԭ���ת��3mol����
C.���������FeΪ��6�ۣ�����ǿ�����ԣ���ɱ������
D.������صĻ�ԭ������ˮ���γɽ��壬��ʹˮ�����������۳���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cu2O�㷺�������Ϻͻ��������Ĵ�����
���Ʊ�Cu2O
��1����ⷨ����ҵ����ͭ����������ƬΪ���������һ��Ũ�ȵ�NaOH ��Һ���Ʊ�������ͭ��д�������ĵ缫��ӦʽΪ_____________________
��2����Һ-��ԭ������ 100�� Cu��NO3��2 ��ˮ��Һ�м���һ������� NaOH ˮ��Һ��������ʹ֮��Ͼ��ȣ� ����μ���ˮ���µ�ˮ��Һ��ֱ��������ɫ�����������ˡ�ϴ�Ӻ���ո���õ�Cu2O ��ĩ��
��֪�� N2H4��l��+O2��g��=N2��g��+2H2O��l����H= -akJ/mol
Cu(OH)2��s��=CuO��s��+H2O��l����H= +bkJ/mol
4CuO��s��=2Cu2O��s��+O2��g����H= +ckJ/mol
����N2H4 ��Cu(OH)2 ��Ӧ�Ʊ� Cu2O ���Ȼ�ѧ����ʽΪ ________________________��
��ҵ����Cu2O �� ZnO ��ɵĴ��������ڹ�ҵ�Ϻϳɼ״��� CO(g)+2H2(g)![]() CH3OH(g) ��H = -90.8 kJ/mol���ش��������⣺
CH3OH(g) ��H = -90.8 kJ/mol���ش��������⣺
��1����˵����ӦCO(g)+2H2(g)![]() CH3OH(g)�Ѵ�ƽ��״̬������_______��
CH3OH(g)�Ѵ�ƽ��״̬������_______��
A������Ӧ����ЧӦ��H = -90.8 kJ/mol ʱ��Ӧ�ﵽƽ��״̬
B.�ں��º�ѹ�������У����������ܶȱ��ֲ���
C.�ھ��Ⱥ��ݵ������У���Ӧ��ƽ�ⳣ�����ٱ仯
D���ں��º��ݵ������У������ƽ��Ħ���������ٱ仯
��2���� T1��ʱ�����Ϊ 2 L �ĺ��������г������ʵ���֮��Ϊ 3mol �� H2 ��CO������ʼ n(H2)��n(CO)= 2 ʱ������ 5min �ﵽƽ�⣬CO ��ת����Ϊ 0.6����0~5min ��ƽ����Ӧ���� v (H2)=___�����¶��µ�ƽ�ⳣ��Ϊ__________________ ������ʱ���������м���CO(g) �� CH3OH(g)�� 0.4mol������ƽ��ʱ H2 ��ת���ʽ� ______������� ����С�����䡱����
��3����ҵʵ�ʺϳ� CH3OH �����У�������ͼM�������N���Ӧ�ķ�Ӧ���������û�ѧ��Ӧ���ʺͻ�ѧƽ��֪ʶ��ͬʱ��������ʵ�ʣ�˵��ѡ��÷�Ӧ���������ɣ�________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ��̼̼������Ȳ������������ּӳɺ�IJ���Ľṹ��ʽΪ��

��Ȳ�����ܵĽṹ��
A.1��B.2��C.3��D.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ��(��)��һ�ֿɳ���أ�װ��(��)Ϊ���ء�װ��(��)�����ӽ���Ĥֻ����Na��ͨ������֪��س䡢�ŵ�Ļ�ѧ����ʽΪ2Na2S2��NaBr3![]() Na2S4��3NaBr�����պϿ���Kʱ��X�缫������Һ��졣����˵����ȷ����
Na2S4��3NaBr�����պϿ���Kʱ��X�缫������Һ��졣����˵����ȷ����
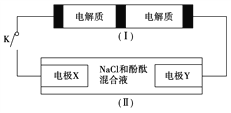
A. �պϿ���Kʱ��Na�����ҵ���ͨ�����ӽ���Ĥ
B. �պϿ���Kʱ��������ӦʽΪ3NaBr��2e��===NaBr3��2Na��
C. �պϿ���Kʱ������0.1 mol Na��ͨ�����ӽ���Ĥʱ��X�缫�Ϸų���״��������1.12 L
D. �պϿ���Kʱ��X�缫��ӦʽΪ2Cl����2e��===Cl2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com