
【题目】Li2O是离子晶体,从如图的BornHaber循环可得出Li2O晶格能为 ( )
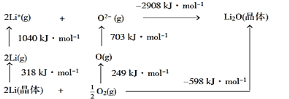
A. 598kJ·mol1B. -598KJ·mol1C. 1168kJ·mol1D. 2908kJ·mol1
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】一种制备N2H4·H2O(水合肼)和无水Na2SO3的主要实验流程如下:

已知:温度超过40 ℃,Cl2与NaOH溶液反应会生成副产物NaClO3。
⑴“反应Ⅰ”中NaOH应过量且同时减慢通入Cl2的速率,目的是______。
⑵常温时,将Cl2通入NaOH溶液中,一段时间后溶液中将有NaClO3生成,原因是______。
⑶写出“反应Ⅱ”中NaClO与(NH2)2CO反应的化学方程式:______。
⑷“反应Ⅲ”中会有气体______(填化学式)生成,检验有该气体的方法是______。
⑸图所示为Na2SO3的溶解度随温度的变化曲线,由质量分数为10%的Na2SO3溶液制取无水Na2SO3的方法是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
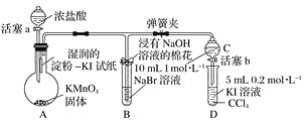
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的离子方程式是____________________________________________。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是____________________________。
(4)过程Ⅲ实验的目的是________________________________________________________。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐________,得电子能力逐渐________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可燃冰是另一种CH4的重要来源,利用可燃冰制备的甲烷可以设计成如下燃料电池,可以作为“移动的发电厂”,源源不断的对外供电,下列说法错误的是

A.a电极通入甲烷气体,作负极
B.每通入1mol CH4,有8mol e-通过质子交换膜
C.b电极的电极反应式为:O2+4e-+4H+=2H2O
D.催化剂电极采用疏松多孔结构可提高电极反应效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元索对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 原于半径:r(Y)>r(Z)>r(W)
B. 化合物N、乙烯使溴水褪色的原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在BaSO4饱和溶液中加入少量的BaCl2溶液产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中
A.c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-)
B.c(Ba2+)=c(SO42-)=(Ksp)1/2
C.c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
D.c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 晶体网状结构(如图)的叙述正确的是
晶体网状结构(如图)的叙述正确的是
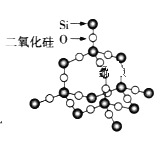
A. 存在四面体结构单元, ![]() 处于中心,
处于中心, ![]() 处于4个顶角
处于4个顶角
B. 最小环上有3个![]() 原子和3个
原子和3个![]() 原子
原子
C. 最小环上![]() 和
和![]() 原子数之比为1:2
原子数之比为1:2
D. 最小环上有6个![]() 原子和6个
原子和6个![]() 原子
原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
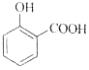 +2HCO3-→
+2HCO3-→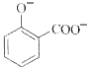 +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com