
一粗铝内含铁和硅两种杂质,取等质量的两份样品,分别投入到足量的稀盐酸和稀NaOH溶液中产生等质量的气体C,已知Al与NaOH溶液反应的化学方程式为2Al+2NaOH+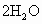 =
=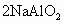 +
+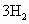 ↑,则该粗铝中硅与铁的质量之比为多少?
↑,则该粗铝中硅与铁的质量之比为多少?
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com