
(1)所得硫酸铜晶体的质量y为__________g(用x表示)。
(2)若x=0.4,则混合酸中HNO3与H2SO4的物质的量之比为__________。
(3)若x=0.4,用
解析:(1)m(CuSO4·5H2O)=[![]() ]×
]×
(2)若x=0.4,在![]() =3 mol
=3 mol
n(CuO)=![]() =3.5 mol
=3.5 mol
依据3Cu+8H++2![]()
![]() 3Cu2++2NO↑+4H2O,所需n(HNO3)=3 mol×
3Cu2++2NO↑+4H2O,所需n(HNO3)=3 mol×![]() =2 mol
=2 mol
n(H2SO4)=3 mol+3.6 mol=6.6 mol,![]()
(3)原混合酸中m(H2SO4)=
所以w(H2SO4)=![]() ×100%=52.6%
×100%=52.6%
答案:(1)375x+ 1 500
(2)10∶33 (3)52.6%


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:
(1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
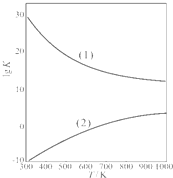 (2011?山西模拟)甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物、涂料等,也是世界卫生组织(WHO)确认的致癌物和致畸物质之一.据中国室内环境监测工作委员会调查统计,中国新装家庭甲醛超标60%以上.我国规定室内空气中甲醛含量不得超过0.08mg/m3.
(2011?山西模拟)甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物、涂料等,也是世界卫生组织(WHO)确认的致癌物和致畸物质之一.据中国室内环境监测工作委员会调查统计,中国新装家庭甲醛超标60%以上.我国规定室内空气中甲醛含量不得超过0.08mg/m3.| 1 | 2 |
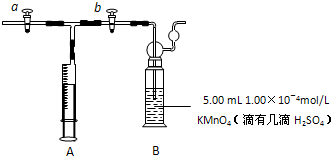
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
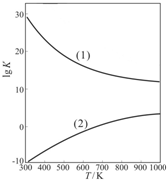
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
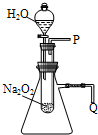 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com