
某实验小组对普通锌锰废干电池内的黑色固体进行探究,设计如下方案:

己知:I、普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。
II、氢氧化锌为白色粉末,不溶于水,溶于酸、强碱溶液和氨水。
请回答以下问题:
(1)②操作的名称是___________。
(2)某同学猜想溶液A的成分含有NH4Cl和ZnCl2,请你设计一个实验方案,验证其猜想正确,要求在答题卡上按下表格式写出实验操作、预期现象和结论。
限选试剂:蒸馏水、2moL·L-1 HCI 、2 moL·L-1 HNO3 、2 moL·L-1 NH3·H2O、6 moL·L-1 NaOH、0.1 moL·L-1 KSCN、0.1 moL·L-1 BaCl2、0.1 moL·L-1 AgNO3、紫色石蕊试液、红色石蕊试纸
|
实验操作 |
预期现象 |
结论 |
|
步骤1:各取少量溶液A分装a、b、c三支试管,往a试管,__ __________________________ |
有白色沉淀产生 |
说明溶液A含有Cl- |
|
步骤2:往b试管,__________ __________________________ |
______________________ |
_______________________ |
|
步骤3:往c试管,__________ __________________________ |
先产生_______________, 后____________________ |
说明溶液A含有Zn2+ |
(3)取少量固体c放入试管,滴加入双氧水,观察到有气体产生,写出该反应的化学方程式:_______________。
(4)为测定废干电池中二氧化锰的质量分数,进行下面实验:准确称取ag废千电池固体,溶于稀硫酸,加入碘化钾溶液,充分反应后,用bmol/L硫代硫酸钠标准溶液滴定,用淀粉作指示剂,滴定至终点,重复实验,平均消耗硫代硫酸钠标准溶液的体积为vmL,则废电池中二氧化锰的质量分数的计算表达式为:________________________________。
(滴定有关反应:MnO2+2I-+4H+=Mn2++I2+2H2O;I2+2S2O32-=2I-+S4O62-)
(17分)
(1)过滤 (2分)
(2)(共11分,试剂不标浓度和用量不准确每空扣1分,用“适量”与“少量”均可,其他合理即给分)
|
实验操作 |
预期现象 |
结论 |
|
步骤1:各取少量溶液A分装a、b、c三支试管,往a试管,滴加适量0.1mol•L-1AgNO3(1分)和2moL•L-1 HNO3 (1分)
|
有白色沉淀产生 |
说明溶液A含有Cl-
|
|
步骤2:往b试管, 加入适量6moL•L-1NaOH(1分)加热(1分),将湿润的红色石蕊试纸置于试管口附近(1分) |
湿润的红色石蕊试纸变蓝色 (1分) |
说明溶液A含有NH4+ (1分) |
|
步骤3:往c试管,逐滴加入2moL•L-1NH3·H2O 或 6moL•L-1NaOH (1分)至过量(1分) |
先产生 白色沉淀 (1分),后 白色沉淀溶解 (1分) |
说明溶液A含有Zn2+ |
(3)
 (2分)
(2分)
(4)
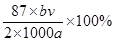 (2分)
(2分)
【解析】
试题分析:(1)依题意,普通锌锰废干电池内的黑色固体加足量蒸馏水溶解时,得到固液不相溶的混合物,二氧化锰不溶于水,氯化铵、氯化锌是可溶性盐,则操作②为过滤,将①所得混合物分离为溶液A和固体B,A的主要成分是氯化铵、氯化锌,B的主要成分是二氧化锰;(2)检验溶液A的主要成分,就是设计实验方案检验是否存在氯离子、铵根离子和锌离子,氯离子常用稀硝酸和硝酸银溶液检验,铵根离子常用热氢氧化钠溶液和湿润的红色石蕊试纸检验,锌离子常用氢氧化钠或氨水检验;步骤1:各取少量溶液A分装a、b、c三支试管,往a试管,滴加适量0.1mol•L-1AgNO3和2moL•L-1 HNO3溶液,产生白色沉淀,说明溶液A含有Cl-;步骤2:往b试管, 加入适量6moL•L-1NaOH、加热,将湿润的红色石蕊试纸置于试管口附近,湿润的红色石蕊试纸变蓝色,说明溶液A含有NH4+;步骤3:步骤3:往c试管,逐滴加入2moL•L-1NH3·H2O 或 6moL•L-1NaOH至过量,先产生 白色沉淀,后白色沉淀溶解,说明溶液A含有Zn2+;(3)二氧化锰固体受热不能分解,则固体C的成分是二氧化锰,双氧水在二氧化锰催化下,分解反应速率增大,生成水和氧气;(4)依题意,由于n=c•V,则硫代硫酸钠的物质的量为bv×10—3mol;由于I2+2S2O32-=2I-+S4O62-中各物质的系数之比等于物质的量之比,则每次滴定消耗的I2为 bv/2×10—3mol;由于MnO2+2I-+4H+=Mn2++I2+2H2O中各物质的系数之比等于物质的量之比,则样品中MnO2为 bv/2×10—3mol;由于二氧化锰的式量为87,m=n•M,则样品中MnO2的质量为87bv/2×10—3g;由于样品的质量为ag,则样品中MnO2的质量分数的表达式为87bv/2a×10—3×100%。
考点:考查探究实验方案的设计和化学计算,涉及混合物分离提纯的方法、设计多种离子的检验方案、过氧化氢的分解反应方程式、测定二氧化锰样品的纯度、滴定、物质的量浓度、溶液体积、物质的量在化学方程式计算中的应用、摩尔质量、质量、质量分数等。


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
(12分)乱扔废旧电池会导致严重的环境污染,一节废电池就是一颗“炸弹”。某化学兴趣小组的同学在探究废干电池内的黑色固体回收利用时,进行了如图所示的实验:
查阅教材可得到下列信息:
① 普通锌锰电池的黑色物质主要成分为MnO2.NH4Cl.ZnCl2等物质。
②Zn(OH)2能溶解于过量的氨水中。
请回答以下问题:
(1)操作③灼烧滤渣时所用到的主要仪器有酒精灯.玻璃棒. .泥三角和三脚架;灼烧滤渣中的黑色固体时,产生一种使澄清的石灰水变浑浊的气体,由此推测滤渣中还存在碳。
(2)操作④的试管中加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为 。
(3)该同学对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 检验Cl- | 取少许滤液于试管中,
|
| 含有Cl- |
| 检验NH4+ | 取少许滤液于试管中,
|
| 含有NH4+ |
| 检验Zn2+ | 取少许滤液于试管中,
|
| 含有Zn2+ |
(4)根据以上实验报告,关于滤液的成分,同学们的结论是:滤液中含有氯化铵和氯化锌,若想从滤液中得到溶质固体,还应进行得操作是 。若要将所得的溶质固体中的物质加以分离,可用 法。
查看答案和解析>>
科目:高中化学 来源:2011届山东省济宁一中高三第一次模拟测试试题理综化学试卷 题型:实验题
(12分)乱扔废旧电池会导致严重的环境污染,一节废电池就是一颗“炸弹”。某化学兴趣小组的同学在探究废干电池内的黑色固体回收利用时,进行了如图所示的实验:

查阅教材可得到下列信息:
①普通锌锰电池的黑色物质主要成分为MnO2.NH4Cl.ZnCl2等物质。
②Zn(OH)2能溶解于过量的氨水中。
请回答以下问题:
(1)操作③灼烧滤渣时所用到的主要仪器有酒精灯.玻璃棒. .泥三角和三脚架;灼烧滤渣中的黑色固体时,产生一种使澄清的石灰水变浑浊的气体,由此推测滤渣中还存在碳。
(2)操作④的试管中加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为 。
(3)该同学对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 检验Cl- | 取少许滤液于试管中, | | 含有Cl- |
| 检验NH4+ | 取少许滤液于试管中, | | 含有NH4+ |
| 检验Zn2+ | 取少许滤液于试管中, | | 含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山东省高三第一次模拟测试试题理综化学试卷 题型:实验题
(12分)乱扔废旧电池会导致严重的环境污染,一节废电池就是一颗“炸弹”。某化学兴趣小组的同学在探究废干电池内的黑色固体回收利用时,进行了如图所示的实验:

查阅教材可得到下列信息:
① 普通锌锰电池的黑色物质主要成分为MnO2.NH4Cl.ZnCl2等物质。
②Zn(OH)2能溶解于过量的氨水中。
请回答以下问题:
(1)操作③灼烧滤渣时所用到的主要仪器有酒精灯.玻璃棒. .泥三角和三脚架;灼烧滤渣中的黑色固体时,产生一种使澄清的石灰水变浑浊的气体,由此推测滤渣中还存在碳。
(2)操作④的试管中加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为 。
(3)该同学对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
|
实验目的 |
操作 |
实验现象 |
结论 |
|
检验Cl- |
取少许滤液于试管中,
|
|
含有Cl- |
|
检验NH4+ |
取少许滤液于试管中,
|
|
含有NH4+ |
|
检验Zn2+ |
取少许滤液于试管中,
|
|
含有Zn2+ |
(4)根据以上实验报告,关于滤液的成分,同学们的结论是:滤液中含有氯化铵和氯化锌,若想从滤液中得到溶质固体,还应进行得操作是 。若要将所得的溶质固体中的物质加以分离,可用 法。
查看答案和解析>>
科目:高中化学 来源: 题型:
乱扔废旧电池会导致严重的环境污染,一节废电池就是一颗“炸弹”。某化学兴趣小组的同学在探究废干电池内的黑色固体回收利用时,进行了如图所示的实验:

查阅教材可得到下列信息:
① 普通锌锰电池的黑色物质主要成分为MnO2.NH4Cl.ZnCl2等物质。
②Zn(OH)2能溶解于过量的氨水中。
请回答以下问题:
(1)操作③灼烧滤渣时所用到的主要仪器有酒精灯.玻璃棒. .泥三角和三脚架;灼烧滤渣中的黑色固体时,产生一种使澄清的石灰水变浑浊的气体,由此推测滤渣中还存在碳。
(2)操作④的试管中加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为 。
(3)该同学对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 检验Cl- | 取少许滤液于试管中,
|
| 含有Cl- |
| 检验NH4+ | 取少许滤液于试管中,
|
| 含有NH4+ |
| 检验Zn2+ | 取少许滤液于试管中,
|
| 含有Zn2+ |
(4)根据以上实验报告,关于滤液的成分,同学们的结论是:滤液中含有氯化铵和氯化锌,若想从滤液中得到溶质固体,还应进行得操作是 。若要将所得的溶质固体中的物质加以分离,可用 法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com