
下列叙述中正确的是( )
A.主族元素的原子核外电子最后填入的能级是d能级或f能级
B.镁型和铜型金属晶体的配位数均为12
C.中心原子上的孤电子对不参与决定分子的空间结构
D.分子中键角越大,价电子对相互排斥力越大,分子越稳定
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:推断题
(14分)带有支链的某烃A的分子式为C6H14,若烃A的一氯取代物只有3种,分别是B、C、D,且有如下的转化。请回答下列问题:
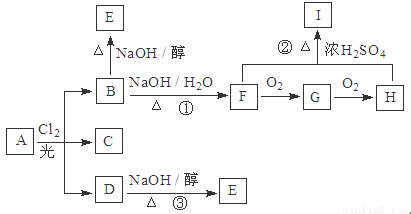
(1)C的名称为________________,G中含有的官能团的名称是______________。
(2)0.1 mol该烃A完全燃烧的产物被碱石灰完全吸收,碱石灰的质量增加__________。
(3)写出下列反应的类型:②_________________;③_________________。
(4)写出D→E的化学方程式_____________________________________________。
(5)H的同分异构体中符合下列条件的共有________种。
①属于酯类化合物;②水解产物含有相同数目的碳原子。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列化学用语正确的是( )
A..聚丙烯的结构简式: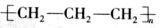
B.四氯化碳分子的电子式:
C.2-乙基-1,3-丁二烯分子的键线式: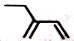
D.丙烷分子的比例模型:
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.碘化铵和氯化铵受热分解过程中破坏和形成的化学键类型完全相同
B.反应N2H4(l)=N2(g)+2H2(g)是一个△S>0的反应
C.1 mol FeCl3完全水解得到的Fe(OH)3胶体中胶粒数目为NA(NA为阿伏加德罗常数)
D.HClO是弱酸,所以NaClO是弱电解质
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:填空题
元素的性质在元素周期表中按其排列呈现一定的规律。下表为元素周期表中部分元素,根据要求回答下列问题:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有 (填元素名称)。
(2)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域:s区、p区、d区、ds区和f区,以上12种元素分别属于s区、d区、ds区和p区,则属于s区的元素有 种,属于d区的元素有 种。
(3)铜晶胞是面心立方结构。其空间利用率为 (用含“π”和“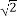 ”的式子表示,不必算结果)
”的式子表示,不必算结果)
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列分子中的中心原子杂化轨道的类型相同的是( )
A.CO2与H2O B.CH4与NH3 C.BeCl2与BF3 D.C2H2与C2H4
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
以下表示氦原子结构的化学用语中,对电子运动状态描述最详细的是( )
A.He : B.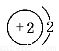 C.1s2 D.
C.1s2 D.
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
下列物质中,既含有极性键又含有非极性键的是:
A.  B . CO2 C . Na2O2 D . NH4Cl
B . CO2 C . Na2O2 D . NH4Cl
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.H2O的熔点、沸点大于H2S的是由于H2O分子之间存在氢键。
B.HF、HCl、HBr、HI的熔点沸点依次升高。
C.乙醇分子与水分子之间只存在范德华力。
D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com